Радикал (хімія)
Радика́л (вільний радикал; від фр. radical та лат. radicalis — «корінний», «той, що має корінь»; від лат. radix, «корінь») в хімії — парамагнітна частинка (атоми або молекули) з неспареним електроном на зовнішній атомній або молекулярній орбіталі.
| Радикал | |
| Участь у | free-radical reactiond |
|---|---|
| | |
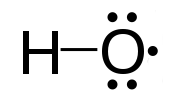
Загальна характеристика ред.
Радикали можуть бути нейтральними або нести позитивний чи негативний заряд. У залежності від характеру орбіталі, яку займає неспарений електрон, розрізняють π-радикали і σ-радикали. У залежності від природи центрального атому (атому з найбільшою спіновою густиною) розрізняють С·, О·, N· та інші атомоцентровані радикали.
Вільні радикали мають непарне число електронів й спін, рівний 1/2; бірадикали мають парне число електронів та спін, рівний 1.
Перший органічний вільний радикал, трифенілметиловий радикал був ідентифікований Мозесом Гомбергом в 1900 році в Мічиганському університеті.
Вільні радикали відіграють важливу роль у горінні, хімічних перетвореннях в атмосфері, полімеризації, хімії плазми, біохімічних та багатьох інших процесах. У біологічних системах вільнорадикальному окисненню можуть підлягати нуклеїнові кислоти, білки, ліпіди та інші речовини, серед цих реакцій особливо важливе значення має перекисне окиснення ліпідів[1]. Деякі вільні радикали, як от супероксид-аніон і моноксид азоту, у багатьох організмів регулюють певні процеси, наприклад зміну тонусу кровоносних судин. Вони також відіграють роль у проміжному метаболізмі різноманітних сполук. Ці радикали можуть бути посередниками у так званому «редокс сигналюванні».
Розрізняють: алкіліденамінильний, алкіліденаміноксильний, алкільний, амінільний, аміноксильнй, аніон- , атомоцентрований, ацилоксильний, вердазильний, вільний, гарячий, діазенільний, імінильний радикал, іміноксильний, йон- , силільний, стабільний, сульфенільний, тропільний фосфоранільний радикал, π-радикал, σ-радикал, радикал-йон.
Радикальний центр (англ. radical centre) — атом (чи група атомів) у багатоатомному радикалі, на якому переважно локалізований неспарений електрон. Залежно від атому, на якому зосереджений неспарений електрон, радикали носять назву С-центрований, О-центрований тощо.
Атомоцентрований радикал (англ. atom centered radical) — термін, що використовується для розрізнення радикалів залежно від того, на якому атомі зосереджений неспарений електрон (тб. вказує на природу атома з найбільшою спіновою густиною), пр., C-, О-, N-центровані радикали.
Ацилоксильний радикал (англ. acyloxyl radical) — оксигенцентрований радикал, які містить ацильну групу, зв'язану з атомом О. Пр., RC(=O)O·, RC(=NR)O·, RS(=O)O·.
Вільні радикали у хімічних реакціях ред.
Вільні радикали можуть виникати під дією тепла, каталізаторів, ультрафіолетового та радіаційного випромінення, інших впливів на молекули. Реакція утворення радикалів називається гомоліз.
Характерна особливість вільних радикалів — висока хімічна активність, обумовлена наявністю вільних валентностей (неспарених електронів). Більшість вільних радикалів мають малу тривалість життя (на рівні декількох мс). Вільні радикали відіграють важливу роль у гетерогенному каталізі, ферментативних процесах у живих організмах, у реакціях швидкого окислення — горіння, у важливих проміжних процесах — крекінгу, піролізу, полімеризації, процесах, які включають механохімічну активацію та ін. Вільні радикали з кінетичною енергією, яка набагато перевищує певне середнє значення, притаманне для нього, називають гарячим радикалом.
Терміни «радикал» і «вільний радикал» іноді використовуються рівнозначно, проте радикал може бути зв'язаний за рахунок ван-дер-вальсівських або інших нековалентних зв'язків.
Органічна хімія вільних радикалів — це хімія парамагнітних парів, рідин, сипучих тіл, розплавів й розчинів[2].
На повітрі органічні речовини зазнають окиснюваних перетворень: понижується теплопровідність рідких й твердих палив, погіршуються характеристики змащувальних масел й гідравлічних рідин, падає міцність виробів з полімерів й пластмас, псуються медикаменти, косметичні засоби, вибухові речовини, жирвмісні корми й харчові продукти. За рациндифікації масла у ньоу накопичуються токсичні продукти окиснюючих реакцій: спирти, карбонільні сполуки, пероксиди, гідропероксиди, оксирани й ін.
Іміноксильні радикали використовуються в якості ефективних інгібіторів реакцій полімеризації, термо- й світлоокиснення різних органічних матеріалів, наприклад, для підвищення стійкості акрилонітрилу, вінілацетату, вінілденхлориду, стиролу, олігоетеракрилатів, фурфуролу, жирів, масел, каротинвмісних кормів. Довгоживучі радикали викоритстовуються для інтенсифікації хемічних процесів, підвищення селективності каталітичних систем й покращення якості при виробництві анаеробних герметиків, епоксидних смол, поліолефінів, метакрилової кислоти. Стабільні парамагнетики взастосовуються у біофізичних й молекулярно-біологічних дослідженнях в якості спінових міток й зондів, у судово-медичній експертизі, аналітичній хемії, для підвищення адгезії полімерних покриттів, у приладобудуванні й дефектоскопії твердих тіл.
Виявлення ред.
Вільні радикали виявляють завдяки їх парамагнітним властивостям. Для цього використовується метод електронно парамагнітного резонансу. Спектри ЕПР дозволяють не лише виявити вільні радикали, але й отримати інформацію про їхню будову й ступінь делокалізації неспареного електрона. Для цього використовують два параметри: g-чинник й константу надтонкого розщеплення. Перший з них є аналогом хемічного зсуву у спектроскопії ЯМР[3].
Протонний обмін між основою та кислотою описується рівнянням:
.
Необхідною умовою для застосування методу ЕПР для спостереження за ходом реакції є наявність магнітно-резонансних параметрів радикалу у формах та . У цьому випадку реакція повинна приводити до частотного обміну між відповідними компонентами спектрів ЕПР радикалі у формах та . Форма лінії сигналу ЕПР у випадку частотного обміну по двом полоенням, які відповідають та -формам радикалу, описується рівнянням:
де — стала; та — часи життя радикалу у формах та відповідно; — різниця частот відповідних ліній у спектрах ЕПР радикалів у формах та ; — часи поперечної релаксації радикалів та . Змінна пов'язана із «сталим» магнітним полем співвідношенням де — напруженість магнітного поля, яка відповідає центру сигналу ЕПР радикалу у формі . У відповідності з цим рівнянням реалізуються різні випадки обміну: швидкий ( ), повільний ( ) та проміжний ( ) у масштабі часу ЕПР. Незалежно від частоти обміну по спектрам ЕПР, можна визначити відношення Визначення часу життя можливе лише у випадку проміжного обміну. Знаючи можна визначити константу рівноваги:
У випадку, коли реакція описує обмін з протоном розчинника ( тобто сольватований протон, рівняння рівноваги пов'язує константу рівноваги із концентрацією протонів що відчиняє можливість використання радикалів в якості -зондів.
Величини визначають як кінетичні параметри реакції , а саме константи швидкостей :
Таким чином, у вказаних випадках аналіз форми сигналу ЕПР дозволяє отримати кількісну інформацію про термодинаміку й кінетику протонного обміну у радикалах[4].
Історичний термін ред.
Історично термін «радикал» також використовувався для опису частин молекули, особливо коли вони залишаються незмінними під час реакцій, таке визначення все ще можна знайти у старих підручниках. Наприклад, метиловий спирт описувався як складова метилового і гідроксильного радикалів. Жоден з цих «радикалів» не був радикалом у сучасному хімічному сенсі, оскільки вони були постійно зв'язані і не мали неспарованих електронів. У мас-спектрометрії, проте, ці групи відділяються у вигляді радикалів під градом високоенергійних електронів та можуть спостерігаються як окремі частинки. Зараз для позначення частин більших молекул використовуються терміни «замісник» або «функціональна група».
У живих організмах ред.
Вільні радикали задіяні у ряді біологічних процесів, зокрема вони необхідні для внутрішньоклітинного знищення бактерій фагоцитами — гранулоцитами і макрофагами. Також ці частинки беруть участь у клітинному сигналюванні (так зване «редокс сигналювання»)[5].
Серед вільних радикалів похідних кисню у біологічних системах найважливішими є супероксид-аніон і гідроксильний радикал, обидва формуються із кисню у відновних умовах. Через високу реакційну здатність ці частинки можуть вступати у небажані взаємодії і шкодити організму. Надмірна концентрація вільних радикалів може призвести до пошкодження і смерті клітин, зокрема під час таких патологічних процесів як рак, інсульт, інфаркт міокарда, цукровий діабет та інші[6].
Вважається, що небажані взаємодії між вільними радикалами і ДНК і викликані ними мутації мутацій, які можуть порушувати проходження клітинного циклу, роблять внесок в утворення злоякісних пухлин[7].
Деякі ознаки старіння також пов'язані із радикалами, наприклад, під час розвитку атеросклерозу вони окиснюють холестерол до 7-кетохолестеролу.[8]. Також вони можуть бути задіяні розвитку хвороби Паркінсона, глухоти, викликаної старінням чи медичними препаратами, шизофренії, хвороби Альцгеймера[9]. Вільнорадикальна гіпотеза старіння стверджує, що саме ці частинки є основною причиною настання старості.
Класичний вільнорадикальний синдром — гемохроматоз (хвороба накопичення заліза) — зазвичай супроводжується набором розладів, пов'язаних із вільними радикалами — порушення руху, психоз, аномалії пігментації шкіри, глухота, артрит і цукровий діабет.
Оскільки, по-перше, вільні радикали необхідні для життя, а по-друге, вони утворюються як побічні продукти метаболізму кисню, в організмів виробився ряд механізмів, що дозволяють протидіяти вільнорадикальним ушкодженням. Це зокрема ферменти супероксиддисмутаза, каталаза, глутатіонпероксидаза і глутатіонредуктаза. Крім цього існує низка неферментних біологічних антиоксидантів: вітаміни A, C і E, поліфеноли, убіхінон, триптофан, фенілаланін, церулоплазмін, трансферин, гаптоглобін[1]. Також існують дані про роль білірубіну і сечової кислоти у процесах знешкодження вільних радикалів[10].
Космохемія ред.
Стабілізовані твердою метрицею радикали зустрічаються у метеоритах, природних мінералах й каустобіолітах. Значення для астронавтики й астрофізики мають розсіяні у міжзірковому просторі «короткоживучі» радикали: й ін., загальна щільність яких досягає г/см3. Дослідження комет вказують на присутність у них радикалів: Судячи по спектрам полярного сяйва, атмосфера землі містить Максимальна концентрація атомів кисню (бірадикал) зафіксована на висоті 105 км над рівнем моря ( на см3). У атмосфері сонця й більш холодних зірок виявлені й інші вільні радикали. Вважають, що мінливе забарвлення поверхні Юпітера обумовлена присутністю у його атмосфері стабілізованих радикалів[11].
Див. також ред.
Примітки ред.
- ↑ а б Ю. В. Абакумова, Н. А. Ардаматский Свободнорадикальное окисление при атеросклерозе как патогенный фактор. Архів оригіналу за 31 березня 2014. Процитовано 7 січня 2014.
- ↑ M. D. Gol'dfeyn, E. G. Rozantsev - FREE RADICALS AND ORGANIC PARAMAGNETICS.
- ↑ Днепровский А. С., Темникова Т. И. Теоретические основы органической химии. — 2-е издание. — Л. : Химия, 1991. — С. 175–198. — ISBN 5-7245-0206-2.
- ↑ Храмцов В.В., Вайнер Л.М. - Реакции переноса протона в свободных радикалах. Спиновые рН-зонды.
- ↑ Pacher P, Beckman JS, Liaudet L (2007). Nitric oxide and peroxynitrite in health and disease. Physiol. Rev. 87 (1): 315—424. doi:10.1152/physrev.00029.2006. PMC 2248324. PMID 17237348.
- ↑ Rajamani Karthikeyan, Manivasagam T, Anantharaman P, Balasubramanian T, Somasundaram ST (2011). Chemopreventive effect of Padina boergesenii extracts on ferric nitrilotriacetate (Fe-NTA)-induced oxidative damage in Wistar rats. J. Appl. Phycol. 23, Issue 2, Page 257 (2): 257—263. doi:10.1007/s10811-010-9564-0.
- ↑ Mukherjee, P. K., Marcheselli, V. L., Serhan, C. N., & Bazan, N. G. (2004). Neuroprotecin D1: A docosahexanoic acid-derived docosatriene protects human retinal pigment epithelial cells from oxidative stress. PNAS. 101 (22): 8491—8496. doi:10.1073/pnas.0402531101. PMC 420421. PMID 15152078.
- ↑ Lyons MA, Brown AJ. (1999). 7-Ketocholesterol. Int J Biochem Cell Biol. 31 (3—4): 369—75. PMID 10224662.
- ↑ Floyd, R. A. (1999). Neuroinflammatory processes are important in neurodegenerative diseases: An hypothesis to explain the increased formation of reactive oxygen and nitrogen species as major factors involved in neurodegenerative disease development. Free Radical Biology and Medicine. 26 (9-10): 1346—1355. doi:10.1016/S0891-5849(98)002937. PMID 10381209.
- ↑ Rhodes C.J. (2000). Toxicology of the Human Environment – the critical role of free radicals. London: Taylor and Francis. ISBN 0-7484-0916-5.
- ↑ Розанцев Э.Г., Гольдфейн М.Д., Пулин В.Ф, - Органические парамагнетики.
Література ред.
- Мала гірнича енциклопедія : у 3 т. / за ред. В. С. Білецького. — Д. : Донбас, 2007. — Т. 2 : Л — Р. — 670 с. — ISBN 57740-0828-2.
- Глосарій термінів з хімії // Й. Опейда, О. Швайка. Ін-т фізико-органічної хімії та вуглехімії ім. Л. М. Литвиненка НАН України, Донецький національний університет. — Донецьк: Вебер, 2008. — 758 с. — ISBN 978-966-335-206-0
- ОКИСНЕННЯ ВІЛЬНОРАДИКАЛЬНЕ [Архівовано 21 лютого 2016 у Wayback Machine.] //Фармацевтична енциклопедія