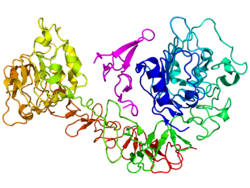
Рецептор епідермального фактора росту
Рецептор епідермального фактора росту (англ. Epidermal growth factor receptor, EGFR) – білок, який кодується однойменним геном EGFR, розташованим у людини на короткому плечі 7-ї хромосоми.[5] Довжина поліпептидного ланцюга білка становить 1 210 амінокислот, а молекулярна маса — 134 277[6].
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MRPSGTAGAA | LLALLAALCP | ASRALEEKKV | CQGTSNKLTQ | LGTFEDHFLS | ||||
| LQRMFNNCEV | VLGNLEITYV | QRNYDLSFLK | TIQEVAGYVL | IALNTVERIP | ||||
| LENLQIIRGN | MYYENSYALA | VLSNYDANKT | GLKELPMRNL | QEILHGAVRF | ||||
| SNNPALCNVE | SIQWRDIVSS | DFLSNMSMDF | QNHLGSCQKC | DPSCPNGSCW | ||||
| GAGEENCQKL | TKIICAQQCS | GRCRGKSPSD | CCHNQCAAGC | TGPRESDCLV | ||||
| CRKFRDEATC | KDTCPPLMLY | NPTTYQMDVN | PEGKYSFGAT | CVKKCPRNYV | ||||
| VTDHGSCVRA | CGADSYEMEE | DGVRKCKKCE | GPCRKVCNGI | GIGEFKDSLS | ||||
| INATNIKHFK | NCTSISGDLH | ILPVAFRGDS | FTHTPPLDPQ | ELDILKTVKE | ||||
| ITGFLLIQAW | PENRTDLHAF | ENLEIIRGRT | KQHGQFSLAV | VSLNITSLGL | ||||
| RSLKEISDGD | VIISGNKNLC | YANTINWKKL | FGTSGQKTKI | ISNRGENSCK | ||||
| ATGQVCHALC | SPEGCWGPEP | RDCVSCRNVS | RGRECVDKCN | LLEGEPREFV | ||||
| ENSECIQCHP | ECLPQAMNIT | CTGRGPDNCI | QCAHYIDGPH | CVKTCPAGVM | ||||
| GENNTLVWKY | ADAGHVCHLC | HPNCTYGCTG | PGLEGCPTNG | PKIPSIATGM | ||||
| VGALLLLLVV | ALGIGLFMRR | RHIVRKRTLR | RLLQERELVE | PLTPSGEAPN | ||||
| QALLRILKET | EFKKIKVLGS | GAFGTVYKGL | WIPEGEKVKI | PVAIKELREA | ||||
| TSPKANKEIL | DEAYVMASVD | NPHVCRLLGI | CLTSTVQLIT | QLMPFGCLLD | ||||
| YVREHKDNIG | SQYLLNWCVQ | IAKGMNYLED | RRLVHRDLAA | RNVLVKTPQH | ||||
| VKITDFGLAK | LLGAEEKEYH | AEGGKVPIKW | MALESILHRI | YTHQSDVWSY | ||||
| GVTVWELMTF | GSKPYDGIPA | SEISSILEKG | ERLPQPPICT | IDVYMIMVKC | ||||
| WMIDADSRPK | FRELIIEFSK | MARDPQRYLV | IQGDERMHLP | SPTDSNFYRA | ||||
| LMDEEDMDDV | VDADEYLIPQ | QGFFSSPSTS | RTPLLSSLSA | TSNNSTVACI | ||||
| DRNGLQSCPI | KEDSFLQRYS | SDPTGALTED | SIDDTFLPVP | EYINQSVPKR | ||||
| PAGSVQNPVY | HNQPLNPAPS | RDPHYQDPHS | TAVGNPEYLN | TVQPTCVNST | ||||
| FDSPAHWAQK | GSHQISLDNP | DYQQDFFPKE | AKPNGIFKGS | TAENAEYLRV | ||||
| APQSSEFIGA |
Білок є мембранним рецептором епідермального фактора росту та є одним з 4 представників родини рецепторів епідермального фактора росту з групи тирозинкіназних рецепторів. Локалізований у клітинній мембрані, ядрі, мембрані, ендоплазматичному ретикулумі, апараті Гольджі, ендосомах. Також секретований назовні.
Бере участь у внутрішньоклітинних сигнальних шляхах, які контролюють клітинний поділ та виживання клітини. Іноді мутації в гені EGFR призводять до збільшення кількості рецептора в раковій клітині. Це призводить до пришвидшення поділу таких клітин. Препарати, які блокують рецептор епідермального фактору росту використовують при лікуванні певних видів злоякісних пухлин.[7]
Окрім власне епідермального фактора росту, рецептор взаємодіє з 6 іншими лігандами:[8]
Література
ред.- Ilekis J.V., Stark B.C., Scoccia B. (1995). Possible role of variant RNA transcripts in the regulation of epidermal growth factor receptor expression in human placenta. Mol. Reprod. Dev. 41: 149—156. PMID 7654368 DOI:10.1002/mrd.1080410205
- Reiter J.L., Maihle N.J. (1996). A 1.8 kb alternative transcript from the human epidermal growth factor receptor gene encodes a truncated form of the receptor. Nucleic Acids Res. 24: 4050—4056. PMID 8918811 DOI:10.1093/nar/24.20.4050
- Ilekis J.V., Gariti J., Niederberger C., Scoccia B. (1997). Expression of a truncated epidermal growth factor receptor-like protein (TEGFR) in ovarian cancer. Gynecol. Oncol. 65: 36—41. PMID 9103388 DOI:10.1006/gyno.1996.4526
- Weber W., Gill G.N., Spiess J. (1984). Production of an epidermal growth factor receptor-related protein. Science. 224: 294—297. PMID 6324343 DOI:10.1126/science.6324343
- Zhang Z., Henzel W.J. (2004). Signal peptide prediction based on analysis of experimentally verified cleavage sites. Protein Sci. 13: 2819—2824. PMID 15340161 DOI:10.1110/ps.04682504
- Huang F., Kirkpatrick D., Jiang X., Gygi S.P., Sorkin A. (2006). Differential regulation of EGF receptor internalization and degradation by multiubiquitination within the kinase domain. Mol. Cell. 21: 737—748. PMID 16543144 DOI:10.1016/j.molcel.2006.02.018
Примітки
ред.- ↑ Захворювання, генетично пов'язані з EGFR переглянути/редагувати посилання на ВікіДаних.
- ↑ Сполуки, які фізично взаємодіють з рецептор епідермального фактора росту переглянути/редагувати посилання на ВікіДаних.
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:3236 (англ.) . Процитовано 7 вересня 2017.
- ↑ UniProt, P00533 (англ.) . Процитовано 7 вересня 2017.
- ↑ epidermal growth factor receptor. NCI's Dictionary of Cancer Terms. National Cancer Institute at the National Institutes of Health(англ.)
- ↑ Arienti C, Pignatta S and Tesei A (2019) Epidermal Growth Factor Receptor Family and its Role in Gastric Cancer. Front. Oncol. 9:1308. doi: 10.3389/fonc.2019.01308
Див. також
ред.| Це незавершена стаття про білки. Ви можете допомогти проєкту, виправивши або дописавши її. |