Пальмітинова кислота
Пальміти́нова кислота́ або ге́ксадека́нова кислота́ (за номенклатурою IUPAC) — це органічна сполука, що належить до ряду жирних кислот. Вона входить до складу усіх гліцеридів органічних жирів та рослинних олій, деяких восків. Неприємний запах пальмітинової кислоти зазвичай відчувається в концентрації вище 10 частин на мільйон, цей запах притаманний людській блювоті. Кислота була відкрита в свинячому салі в 1816 році французьким хіміком Шеврелем.
| Пальмітинова кислота | |
|---|---|
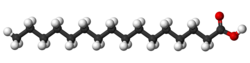
| |
| Назва за IUPAC | Гексадеканова кислота |
| Ідентифікатори | |
| Номер CAS | 57-10-3 |
| Номер EINECS | 200-312-9 |
| DrugBank | DB03796 |
| KEGG | D05341 і C00249 |
| Назва MeSH | D10.251.694.750 |
| ChEBI | 15756 |
| SMILES | CCCCCCCCCCCCCCCC(=O)O |
| InChI | InChI=1S/C16H32O2/c1-2-3-4-5-6-7-8-9-10-11-12-13-14-15-16(17)18/h2-15H2,1H3,(H,17,18) |
| Номер Бельштейна | 607489 |
| Номер Гмеліна | 190200 |
| Властивості | |
| Молекулярна формула | C15H31COOH |
| Молярна маса | 256,424 г/моль |
| Зовнішній вигляд | білі кристали |
| Густина | 0,8527 г/см³[1][2] |
| Тпл | 62,5 °C |
| Ткип | 351,5 °C[2] |
| Розчинність (вода) | 0,0072 г/л[3] |
| Діелектрична проникність (ε) | 2,417 |
| Показник заломлення (nD) | 1,43345[4] |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 |
-891,5 кДж/моль[5][6] |
| Ст. ентропія S 298 |
452,4 Дж/(моль·K)[5] |
| Теплоємність, c p |
450,7 Дж/(моль·K)[5] |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Пальмітинова кислота є сировиною для виробництва складових мила.
Поширення у природі
ред.Пальмітинова кислота є однією з найпоширеніших жирних кислот. Вона входить до складу великої кількості рослинних олій, а також до складу гліцеридів жирних кислот.
Найбільший її вміст спостерігається в пальмовій олії, яка і дала назву сполуці:
| Джерело | Вміст, % |
|---|---|
| Пальмова олія | 38—48 |
| Кава | 25—35 |
| Бавовняна олія | 17—29 |
| Олія камелії | >16 |
| Арахісова олія | 6—16 |
| Олія дині | 12 |
| Лляна олія | 5—8 |
Отримання
ред.Найпоширенішим методом отримання пальмітинової кислоти є гідроліз жирів. За температури менше 100 °C активність процесу є низькою, вона досягає необхідного рівня лише при 210 °C. Тому у виробництві застосовуються хімічні каталізатори: ароматичні вуглеводні, концентрована сульфатна кислота. За їхньої присутності і температурі 100 °C, гідроліз відбувається протягом 12—24 годин.
Застосування біологічних каталізаторів, ліпаз, дає змогу проводити реакцію за температур менше 50 °C, що є значною перевагою в енергозаощадженні і можливістю проводити розщеплення термочутливих жирів.
Пальмітинова кислота також може бути отримана ректифікацією або дробною кристалізацією із суміші жирних кислот, зокрема синтетичних.
Біосинтез
ред.Пальмітинова кислота є одним із головних продуктів синтезу жирних кислот у рослин і тварин. Синтез починається за участі ацетилкоеферменту А, який утворюється з вуглеводів. Поступовим «додаванням» молекул ацетил КоА, ланцюг кислоти щоразу збільшується на парну кількість атомів карбону.
За такою схемою переважно утворюється саме пальмітинова кислота, із незначними домішками лауринової, міристинової і стеаринової кислот.
Пальмітинова кислота і здоров'я
ред.Надмірне споживання пальмітинової кислоти, яка наприклад становить 44 % від складу пальмової олії, підвищує рівень ліпопротеїнів низької густини (ЛПНГ) і загального холестерину в крові, отже підвищує ризик серцево-судинних захворювань.[7][8] Інші установи, Всесвітня організація охорони здоров'я та Національний інститут серця, легенів і крові США, закликали споживачів обмежити споживання пальмової олії, пальмітинової кислоти та продуктів з високим вмістом насичених жирів.[9][10]
Застосування
ред.Пальмітинова кислота здебільшого застосовується для отримання солей, які входять до складу мила (наприклад, пальмітат натрію).
Вона є вихідною сполукою для синтезу деяких двохосновних карбонових кислот. Окисненням кислоти оксидом N2O4, утворюється коркова (октандіова) кислота C8H14O4, а озонолізом цієї сполуки синтезують бурштинову (C4H6O4) та азелаїнову (C9H16O4) кислоти.
Алюмінієві солі нафтенових та пальмітинових кислот використовувались протягом Другої Світової війни для виробництва напалму (термін напалм походить від слів нафтенові та пальмітинові кислоти).
Див. також
ред.Примітки
ред.- ↑ При 62 °C
- ↑ а б За тиску 101,3 кПа
- ↑ При 20 °C
- ↑ При 60 °C
- ↑ а б в Для твердої речовини
- ↑ Для кислоти у рідкому та газуватому станах теплоти утворення дорівнюють -838,1 та -737,1 кДж/моль відповідно
- ↑ ORIGINAL ARTICLE Quantitative effects on cardiovascular risk factors and coronary heart disease risk of replacing partially hydrogenated vegetable oils with other fats and oils (PDF).
- ↑ Sacks, Frank M.; Lichtenstein, Alice H.; Wu, Jason H.Y.; Appel, Lawrence J.; Creager, Mark A.; Kris-Etherton, Penny M.; Miller, Michael; Rimm, Eric B.; Rudel, Lawrence L. (18 липня 2017). Dietary Fats and Cardiovascular Disease: A Presidential Advisory From the American Heart Association. Circulation. Т. 136, № 3. с. e1—e23. doi:10.1161/CIR.0000000000000510. Процитовано 22 червня 2022.
- ↑ (PDF) https://www.freezepage.com/1348239076FHWAJDADVT?url=http://whqlibdoc.who.int/trs/who_trs_916.pdf. Архів оригіналу (PDF) за 21 вересня 2012. Процитовано 22 червня 2022.
{{cite web}}: Пропущений або порожній|title=(довідка) - ↑ Cruel Oil. Center for Science in the Public Interest (англ.). Процитовано 22 червня 2022.
Джерела
ред.- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5.
- Thomas A. Fats and Fatty Oils // Ullmann's Encyclopedia of Industrial Chemistry. — 6th. — Weinheim : Wiley-VCH, 2005. — 73 p. — DOI:
- Anneken D. J., Both S., Christoph R., Fieg G., Steinberner U., Westfechtel A. Fatty Acids // Ullmann's Encyclopedia of Industrial Chemistry. — 6th. — Weinheim : Wiley-VCH, 2005. — 29 p. — DOI:
- Химический энциклопедический словарь / И. Л. Кнунянц. — М. : Сов. энциклопедия, 1983. — 792 с.