Нафтален
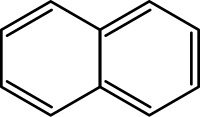
Нафталéн, також нафталíн — найпростіший представник вуглеводнів з конденсованими ароматичними кільцями.
| Нафтален | |
|---|---|
| |

| |
| Назва за IUPAC | біцикло[4.4.0]дека-1,3,5,7,9-пентен |
| Інші назви | нафталін, камфорна смола, біла смола, albocarbon, antimite, moth flakes |
| Ідентифікатори | |
| Номер CAS | [1] 91-20-3[1] |
| PubChem | [1] 931[1] |
| Номер EINECS | 202-049-5[1] |
| KEGG | C00829 |
| ChEBI | 16482 |
| RTECS | QJ0525000[1] |
| SMILES | c1ccc2ccccc2c1 |
| InChI | 1/C10H8/c1-2-6-10-8-4-3-7-9(10)5-1/h1-8H[1] |
| Номер Бельштейна | 1421310 |
| Номер Гмеліна | 3347 |
| Властивості | |
| Молекулярна формула | C10H8 |
| Молярна маса | 128,17 г/моль |
| Зовнішній вигляд | Білі кристали або пластівці, характерний різкий запах[1] |
| Густина | 1,15 г/см³[1] |
| Тпл | 80.26[1] |
| Ткип | 218[1] |
| Розчинність (вода) | 31 мг/л[1] |
| Небезпеки | |
| ЛД50 | 533 мг/кг (миші, орально)[1] |
| ГГС піктограми | 
|
| ГГС формулювання небезпек | H228, H302, H351, H410 |
| ГГС запобіжних заходів | P201, P202, P264, P270, P273, P281, P301+P312, P308+P313
, P330, P391, P405, P501 |
| R-фрази | R22, R40, R50/53[2] |
| S-фрази | S2, S36/37/39, S45, S46, S60, S61[2] |
| Головні небезпеки | легкозаймистий, чутливий до удару, можливий канцероген. Пил може утворювати вибухонебезпечні суміші з повітрям[2] |
| NFPA 704 | |
| Температура спалаху | 80 °C[2] |
| Температура самозаймання | 540 °C[2] |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Історія
ред.Був відкритий у кам'яновугільній смолі А. Гарденом в 1819 р. Елементний склад його встановив О. А. Воскресенський у 1838 році, структурну формулу запропонував Е. Ерленмейєр у 1866 році, а К. Гребе підтвердив її хімічним шляхом у 1868 році[3].
Фізичні властивості
ред.Біла кристалічна речовина, дуже летка та легко сублімується[1].
Будова
ред.Молекула нафталіну складається з двух конденсованих бензольних кілець. Атоми вуглецю у молекулі нафталену нумеруются наступним чином:
Атоми вуглецю, які не зв'язані з атомами водню, не нумеруються, тому що до них не може приєднатися замісник.
Будова нафталену виражається резонансними структурами:
З резонансних структур видно, що не всі зв'язки є рівними. Наприклад, у двох з трьох резонансних структур зв'язок С2-С3 є одинарним, а в одній — подвійним. А зв'язок С1-С2 у двох структурах подвійний, а в одній — одинарний, тому він є більш ненасиченим за С2-С3.
Це підтверджується довжинами зв'язків: відомо, що довжина зв'язку С1-С2 дорівнює 135,6 пм, а зв'язку C2-C3 — 142,5 пм, а чим коротший зв'язок, тим більша його ненасиченість.
Усе це свідчить про те, що нафтален є менш ароматичним, ніж бензен, деякі зв'язки є більш ненасиченими. Через це нафтален легше вступає у реакції приєднання[3].
Отримання
ред.Нафтален отримують з кам'яновугільної смоли, його вміст у фракції 210–230 °C досягає 40 %.
Продукти риформінгу нафти містять багато метилнафталену. З нього нафтален можна отримати при гідродеметилюванні: приєднанні водню, коли один атом приєднується до метильної групи, утворюючи метан, а інший — до нафталенового ядра з утворенням нафталену. Реакцію проводять при температурі 750 °C у присутності каталізаторів — кобальту або молібдену.
Нафтален також утворюється при конденсації бензену та ацетилену:
Ще один спосіб отримання — дієновий синтез. При взаємодії 1,4-бензохінону з бутадієном утворюється тетрагідронафтохінон. Спочатку його дегідрують (утворюється 1,4-нафтохінон), а далі відновлюють воднем у присутності платини.
Хімічні властивості
ред.Нафталіну найбільш притаманні реакції електрофільного заміщення.
Електрофільне заміщення
ред.Переважно заміщується в α-положення (1,4,5,8 атоми вуглецю), оскільки так при делокалізації позитивного заряду, який утворюється при приєднанні електрофіла до ненасиченого зв'язку, ароматична структура іншого кільця не порушується. Також, у α-положеннях є надлишок електронної густини, тобто вони є нуклеофільними. При β-заміщенні позитивний заряд може переходити до іншого ядра, і його структура перетвориться на хіноїдну.[3]
Галогенування
ред.Галогенування проходить дуже легко. При бромуванні, наприклад, утворюється α-бромонафтален, а при надлишку брому утворюється суміш 1,4- та 1,5- дибромонафталенів[4]. Реакція галогенування проходить при 50–70°С за механізмом приєднання-відщеплення: спочатку молекула галогену приєднується (у положення 1,4), а потім відбувається дегідрогалогенування.[3]
При застосуванні таких каталізаторів, як FeCl3, галогенування проходить за механізмом електрофільного заміщення:
При цьому у кінцевому продукті 90–95 % α-ізомеру.[3]
Нітрування
ред.Нітрування проводять 100 % нітратною кислотою у присутності сульфатної кислоти при 50–60 °C. Вміст β-нафталену не перевищує 5 %. Друга нітрогрупа заміщує атом водню у іншому кільці, у положеннях 5 (33 %) та 8 (67 %), оскільки нітрогрупа є електроноакцепторною і дезактивує перше кільце[3].
Сульфування
ред.При сульфуванні за температури 80 °C утворюється α-нафталенсульфонова кислота, яка при нагріванні до 160 °C переходить у β-ізомер[3][4].
Це пов'язано з тим, що α-ізомер утворюється з більшою швидкістю, проте β-ізомер є більш стабільним. При 80 °C напрямок реакції залежить від швидкості, тобто це умови кінетичного контролю. За умов термодинамічного контролю утворюється біль стійка β-нафталенсульфонова кислота[3][4].
Ацилювання
ред.Ацилюється нафтален легше за бензен та толуен. Каталізатором може бути хлорид алюмінію. Який утворюється ізомер — залежить від розчинника: при застосуванні сірковуглецю утворюється α-ізомер, а при застосуванні нітробензену — β-ізомер[3].
Нуклеофільне заміщення
ред.Для реакцій нуклеофільного заміщення також характерне утворення переважно α-похідних. Похідні нафталену вступають у ці реакції краще, ніж сам нафтален. Може взаємодіяти з амідом натрію (NaNH2), що не властиво незаміщеному бензену[3].
Приєднання
ред.Внаслідок меншої ароматичності та більшої ненасиченості порівняно з бензеном, нафтален легше, ніж бензен, входить до реакцій приєднання. Водень приєднує у присутності нікелю. При 200 °C утворюється 1,2,3,4-тетрагідронафталін[en] (тетралін), а при 300 °C всі зв'язки насичуються[3].
Може також приєднувати дієнофіли[3].
Окиснення
ред.Окиснюється нафтален легше, ніж бензен. Під дією хромової суміші при 25 °C утворюється 1,4-нафтохінон. При окисненні 2-метилнафталену окиснюється лише ядро, а CH3-група залишається, на відміну від толуену[3].
У присутності оксиду ванадію(V) утворюється фталевий ангідрид[3]:
Застосування
ред.Свого часу нафтален застосовували як інсектицид,[5] зокрема, для боротьби з міллю: одяг для тривалого зберігання пересипали нафталеном. Звідси походить фразеологізм «витягти з нафталіну».[6]
У XXI сторіччі нафтален знаходить основне застосування в хімічному синтезі як сировина для отримання фталевого ангідриду, декаліну[en], тетраліну, нафтолів, нафтиламінів тощо,[5] в синтезі азобарвників, поверхнево-активних речовин, репелентів, пластифікаторів.[7]
Токсичність
ред.Нафтален подразнює очі, вдихання нафталену призводить до гемолізу. У важких випадках зв'являється гемоглобінурія (поява гемоглобіну у сечі) та метгемоглобінемія (поява великої кількості метгемоглобіну у крові).[1]
За класифікацією IARC, належить до канцерогенів групи 2B.[1][2]
Примітки
ред.- ↑ а б в г д е ж и к л м н п р PubChem. Naphthalene. pubchem.ncbi.nlm.nih.gov (англ.). Процитовано 30 серпня 2020.
- ↑ а б в г д е ICSC 0667 - NAPHTHALENE. ilo.org.
- ↑ а б в г д е ж и к л м н п р Ластухін, Юрій Олександрович; Воронов, Станіслав Андрійович (2009). Органічна хімія. Львів: Центр Європи. с. 753. ISBN 966-7022-19-6.
- ↑ а б в Нейланд, О.Я. (1990). Органическая химия (російська) . Москва: Высшая школа. с. 202-206. ISBN 5-06-001471-1.
- ↑ а б Нафталин // Химическая энциклопедия : в 5 т. / гл. ред. И. Л. Кнунянц. — М. : Большая Рос. энцикл., 1992. — Т. 3 : Меди сульфиды — Полимерные красители. — Стб. 371. — Библиогр. в конце ст. — ISBN 5-85270-039-8.(рос.)
- ↑ Нафталін // Словник української мови : у 20 т. — К. : Наукова думка, 2010—2022.
- ↑ Collin G.; Höke H.; Greim H. (2003). Naphthalene and Hydronaphthalenes. Ullmann's Encyclopedia of Industrial Chemistry. doi:10.1002/14356007.a17_001.pub2.



