Фторсульфонова кислота
Фторсульфо́нова кислота́ (назва за IUPAC: су́льфорофтори́дна кислота́) — неорганічна сполука з хімічною формулою HSO3F. Це одна з найсильніших комерційно доступних кислот.
| Фторсульфонова кислота | |
|---|---|
 Скелетна формула
|
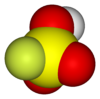 Просторова модель
|

| |
| Назва за IUPAC | Сульфорофторидна кислота |
| Систематична назва | Фторсульфатна кислота[джерело?] |
| Інші назви | Фторсульфатна кислота, Флюорсульфатна кислота, Флюорсульфонова кислота, Фторидсульфонова кислота, Фторидсульфатна кислота, Фторгідрин сульфат |
| Ідентифікатори | |
| Номер CAS | 7789-21-1 |
| PubChem | 24603 |
| Номер EINECS | 232-149-4 |
| Назва MeSH | Fluorosulfonic+acid |
| RTECS | LP0715000 |
| SMILES | OS(F)(=O)=O |
| InChI | 1/FHO3S/c1-5(2,3)4/h(H,2,3,4) |
| Властивості | |
| Молекулярна формула | FHO3S |
| Зовнішній вигляд | Безбарвна димляча рідина |
| Густина | 1,726 г/см−3 |
| Кислотність (pKa) | -10 |
| Структура | |
| Координаційна геометрія |
Тетрагональна на S |
| Геометрія | Тетрагідральна на S |
| Небезпеки | |
| ГГС піктограми |  
|
| ГГС формулювання небезпек | 314, 332
} |
| ГГС запобіжних заходів | 280, 305+351+338, 310 |
| NFPA 704 | |
| Пов'язані речовини | |
| Пов'язані речовини | Пентафторид стибію, Трифторметансульфонова кислота, Плавикова кислота, Сірчана кислота, Гексафторид сірки |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Це тетраедрична молекула, яка тісно пов'язана з сірчаною кислотою, H2SO4, заміщаючи атом фтору замість однієї з гідроксильних груп.
Дана кислота є безбарвною рідиною, хоча комерційні зразки часто мають жовтий колір.[1]
Властивості ред.
Фторсульфонова кислота — сипуча безбарвна рідина. Вона розчинна у полярних органічних розчинниках (наприклад, нітробензен, оцтова кислота та етилацетат), але погано розчинна у неполярних розчинниках, таких як алкани.
HSO3F є однією з найсильніших відомих простих кислот Бренстеда.[2] Вона має значення H0 -15,1 порівняно з −12 сірчаної кислоти. Поєднання фторсульфонової кислоти і кислоти Льюїса пентафториду стибію дає «магічну кислоту», яка є набагато сильнішим протонуючим агентом. Такі кислоти класифікуються як «суперкислоти» ― кислоти, що сильніші за 100 % сірчану кислоту.
Відображаючи її сильну кислотність, HSO3F розчиняє майже всі органічні сполуки, які є навіть слабкими акцепторами протонів.[3] HSO3F повільно гідролізується до фтороводню (HF) і сірчаної кислоти (H2SO4). Споріднена трифлієва кислота (CF3SO3H) зберігає високу кислотність HSO3F, але є більш гідролітично стабільною. Також відбувається самоіонізація фторсульфонової кислоти:
- 2HSO3F ⇌ [H2SO3F]+ + [SO3F]− K = 4,0 × 10−8 при 298°K (24.8 °C)
HSO3F ізомеризує алкани та каталізує алкілування вуглеводнів алкенами[4], хоча неясно, чи такі застосування мають комерційне значення. ЇЇ також можна використовувати як лабораторний фторуючий агент.[5]
Отримання ред.
Фторсульфонову кислоту отримують за допомогою реакції фтороводню і триоксиду сірки:
- SO3 + HF → HSO3F
Крім того, KHF2 або CaF2 можна обробити олеумом при 250 °C. Після звільнення від фтороводню шляхом прибирання за допомогою інертного газу, HSO3F можна дистилювати в скляному апараті.[5]
Безпека ред.
Фторсульфонова кислота вважається високотоксичною та надзвичайно корозійною. Вона гідролізується з виділенням фтористого водню. При додаванні води до фторсульфонової кислоти може бути бурхлива реакція, подібна до додавання води до сірчаної кислоти, але набагато сильніша.
Див. також ред.
- Хлорсульфатна кислота
- Сульфурилфторид
- Метилфторсульфонат, органічний ефір фторсульфонової кислоти
- Трифторметилсульфонова кислота
Примітки ред.
- ↑ Erhardt Tabel, Eberhard Zirngiebl, Joachim Maas «Fluorosulfuric Acid» in «Ullmann's Encyclopedia of Industrial Chemistry» 2005, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a11_431
- ↑ Christopher A. Reed «Myths about the Proton. The Nature of H+ in Condensed Media» Acc. Chem. Res., 2013, 46 (11), pp 2567—2575. DOI:10.1021/ar400064q
- ↑ Olah, G. A.; Prakash, G. K.; Wang, Q.; Li, X.-Y. (2001). Encyclopedia of Reagents for Organic Synthesis. Encyclopedia of Reagents for Synthesis. John Wiley & Sons. doi:10.1002/047084289X.rf014. ISBN 0471936235.
- ↑ Olah, G.; Farooq, O.; Husain, A.; Ding, N.; Trivedi, N.; Olah, J. (1991). Superacid HSO3F/HF-Catalyzed Butane Isomerisation. Catalysis Letters. 10 (3–4): 239—247. doi:10.1007/BF00772077.
- ↑ а б Cotton, F. A.; Wilkinson, G. (1980). Advanced Inorganic Chemistry (вид. 4th). New York: Wiley. с. 246. ISBN 0-471-02775-8.
