Такролімус
| Зауважте, Вікіпедія не дає медичних порад! Якщо у вас виникли проблеми зі здоров'ям — зверніться до лікаря. |
| Ця стаття містить правописні, лексичні, граматичні, стилістичні або інші мовні помилки, які треба виправити. (березень 2015) |
| Ця стаття потребує додаткових посилань на джерела для поліпшення її перевірності. (березень 2015) |
Такролімус (торгова назва Prograf, Advagraf, Protopic) це імуносупресивний препарат, який використовується, головним чином, після трансплантації алогенних органів, щоб знизити активність імунної системи пацієнта і знизити ризик відторгнення органів. Він також використовується в актуальних препаратів при лікуванні атопічного дерматиту (екземи), важкої вогнетривкої увеїт після трансплантації кісткового мозку, загострень мінімальної захворювання зміни, Th2-опосередкованих захворювань, таких як хвороба Кімури, і стан шкіри вітіліго.
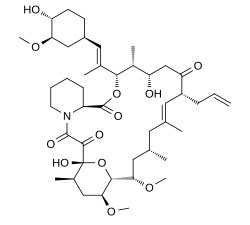
| |

| |
| Систематична назва (IUPAC) | |
| 3S-[3R*[E(1S*,3S*,4S*)] ,4S*,5R*,8S*,9E,12R*,14R*,15S*,16R*,18S*,19S*,26aR* | |
| Ідентифікатори | |
| Номер CAS | |
| Код ATC | |
| PubChem | |
| DrugBank | |
| Хімічні дані | |
| Формула | C44H69NO12 |
| Мол. маса | 804.018 g/mol |
| SMILES | & |
| Фармакокінетичні дані | |
| Біодоступність | 20%, less after eating food rich in fat |
| Зв'язування | 75-99% |
| Метаболізм | Hepatic CYP3A4, CYP3A5 |
| Період напіврозпаду | 11.3 h (range 3.5-40.6 h) |
| Виділення | Mostly faecal |
| Терапевтичні застереження | |
| Кат. вагітності | |
| Лег. статус |
℞ Prescription only |
| Шляхи введення | Topical, oral, внутрішньовенно |
Це 23-членний макролід лактон виявлений у 1984 році з ферментаційного бульйону японського зразка ґрунту, який містив бактерії Streptomyces tsukubaensis.
Історія
ред.Таколімус був виявлений у 1987 р.[1] він був одним з перших макролідних імунодепресантів, виявлених, перед відкриттям рапаміцину (сиролімусу) на Рапа-Нуї (Острів Пасхи) у 1975 році[2]. Він проводиться за типом ґрунтової бактерії, Streptomyces tsukubaensis[3]. Назва такролімус походить від «Цукуба макролідів іммуносупрессанта»[4].
Такролімус був вперше схвалений з контролю за продуктами і ліками у 1994 році для використання в трансплантації печінки; потім було розширена, щоб включити нирку, серце, тонкої кишки, підшлункової залози, легень, трахеї, шкіра, рогівка, кістковий мозок, і трансплантації кінцівок.
Фармакологічні властивості
ред.Фармакодинаміка.
ред.На молекулярному рівні ефекти Такролімусу зумовлюються зв'язуванням з цитозольним білком (FKBP12), який відповідає за внутрішньоклітинну акумуляцію препарату. Комплекс FKBP12-такролімус специфічно та конкурентно зв'язується з кальциневрином та інгібує його, що призводить до кальцій залежного інгібування Т-клітинних сигнальних шляхів трансдукції, таким чином запобігає транскрипції дискретної групи лімфокінних генів. Такролімус являє собою високоактивний імуносупресивний препарат, який пригнічує формування цитотоксичних лімфоцитів, які, в основному, відповідають за відторгнення трансплантата, знижують активацію Т-клітин, залежну від Т-хелперів проліферацію В-клітин, а також формування лімфокінів (таких як інтерлейкіни-2, −3 та g-інтерферон), експресію рецептора інтерлейкіну-2.
Фармакокінетика.
ред.Абсорбція.
ред.Такролімус абсорбується зі шлунково-кишкового тракту; основним місцем абсорбції є верхній відділ шлунково-кишкового тракту. Концентрації (Сmах) Такролімусу в крові досягають піка приблизно через 1-3 год. У деяких пацієнтів препарат абсорбується тривалий період, досягаючи відносно рівного профілю абсорбції. Середнє значення параметрів абсорбції наведено нижче: Популяція Дозування (мг/кг/добу) Сmaх (нг/мл) Тmaх (година) Біодоступність (%) Трансплантат печінки дорослої людини (рівноважна концентрація) 0,30 74,1 3,0 21,8 (± 6,3) Трансплантат печінки дитини (рівноважна концентрація) 0,30 37,0 (± 26,5) 2,1 (± 1,3) 25 (± 20) Трансплантат нирки дорослої людини (рівноважна концентрація) 0,30 44,3 (± 21,9) 1,5 20,1 (± 11,0) Після перорального застосування (0,30 мг/кг/добу) препарату пацієнтами з трансплантатом печінки у більшості хворих рівноважні концентрації Такролімусу досягались протягом 3 днів. У пацієнтів з трансплантатом печінки в стабільному стані біодоступність Такролімусу знижувалась при пероральному застосуванні препарату після вживання їжі з помірним вмістом жирів. Було відзначено також зниження площі під фармакокінетичною кривою AUC (27%), максимальної концентрації Сmах (50%) та збільшення Tmax (173%) в нерозведеній крові. При одночасному застосуванні препарату з їжею знижувалась швидкість та ступінь абсорбції Такролімусу. Виділення жовчі не впливає на абсорбцію Такролімусу. Спостерігається сильна кореляція між AUC та мінімальними рівнями препарату в нерозведеній крові при досягненні рівноважного стану, через що моніторинг мінімальних рівнів препарату в нерозведеній крові може допомогти в адекватній оцінці системного впливу препарату. Розподіл У системному кровотоці Такролімус значною мірою зв'язується з еритроцитами. Співвідношення нерозведена кров/плазмова концентрація становить десь 20:1. У плазмі крові препарат значною мірою зв'язується (> 98,8%) з білками, в основному, із сироватковими альбуміном та α-1-кислим глікопротеїном. Такролімус широко розподіляється в організмі. Рівноважний об'єм розподілу на основі плазмових концентрацій становить приблизно 1 300л (здорові добровольці). Відповідний показник на основі нерозведеної крові в середньому 47,6 л. Такролімус — препарат з низьким рівнем кліренсу. У здорових добровольців середнє значення загального кліренсу, який оцінюється за концентраціями препарату в нерозведеній крові, становить 2,25 л/год. У дорослих пацієнтів з трансплантатом печінки та нирок значення цього параметра становили 4,1 л/год та 6,7 л/год, відповідно. У дітей з трансплантатом печінки значення загального кліренсу приблизно в 2 рази вище, ніж у дорослих хворих з трансплантатом печінки. Період напів виведення Такролімусу є тривалим та змінним. У здорових добровольців середнє значення періоду напів виведення з нерозведеної крові становить приблизно 43 год. У дорослих пацієнтів та дітей з трансплантатом печінки період напів виведення в середньому становить 11,7 год та 12,4 год, відповідно, порівняно з 15,6 год у дорослих пацієнтів з трансплантатом нирки. Метаболізм При використанні in vitro моделей виявлені вісім метаболітів, серед яких тільки один метаболіт має істотну імуносупресивну активність. Такролімус значною мірою метаболізується печінковим мікросомальним цитохромом Р4503А 4 ізоензимом (CYP3A4). Елімінація Після перорального введення такролімусу, міченого 14С ізотопом, більшість радіо активно міченого препарату виводилося з фекаліями. Приблизно 2% виводиться з сечею. Менше 1% незміненого Такролімусу було виявлено в сечі та фекаліях, що вказує на те, що Такролімус практично повністю метаболізується до елімінації. Основним шляхом елімінації є жовч.
Посилання
ред.- ↑ Kino, T.et al.FK-506, a novel immunosuppressant isolated from aStreptomyces.1. Fermentation, isolation, and physico-chemical and biological characteristics. J. Antibiot.40,1249-1255 (1987).
- ↑ Kino T, Hatanaka H, Hashimoto M, Nishiyama M, Goto T, Okuhara M, Kohsaka M, Aoki H, Imanaka H (1987). «FK-506, a novel immunosuppressant isolated from a Streptomyces. I. Fermentation, isolation, and physico-chemical and biological characteristics.». J Antibiot (Tokyo) 40 (9): 1249-55. doi:10.7164/antibiotics.40.1249. PMID 2445721.
- ↑ Pritchard D (2005). «Sourcing a chemical succession for cyclosporin from parasites and human pathogens.». Drug Discov Today 10 (10): 688-91. doi:10.1016/S1359-6446(05)03395-7. PMID 15896681.
- ↑ Ponner, B, Cvach, B (Fujisawa Pharmaceutical Co.): Protopic Update 2005