Нікотинова кислота
Нікоти́нова кислота́, також ніацин, вітамін B3, вітамін PP (від англ. pellagra preventing), нікотинамід — розчинний у воді вітамін; необхідний для багатьох реакцій окиснення у живих клітинах.
| Нікотинова кислота | |
|---|---|
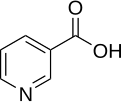 Структурна формула ніацину
|
 Кулькова модель ніацину
|
| Назва за IUPAC | pyridine-3-carboxylic acid[1] |
| Систематична назва | Pyridine-3-carboxylic acid[2] |
| Інші назви | Bionic Vitamin B3 |
| Ідентифікатори | |
| Номер CAS | 59-67-6 |
| PubChem | 938 |
| Номер EINECS | 200-441-0 |
| DrugBank | DB00627 |
| KEGG | D00049 |
| Назва MeSH | Niacin |
| ChEBI | 15940 |
| RTECS | QT0525000 |
| SMILES | Oc(:o): c1cccnc1 |
| InChI | 1/C6H5NO2/c8-6(9)5-2-1-3-7-4-5/h1-4H, (H,8,9) |
| Номер Бельштейна | 109591 |
| Номер Гмеліна | 3340 |
| 3DMet | B00073 |
| Властивості | |
| Молярна маса | 123,1094 г/моль |
| Молекулярна маса | 123,032028409 г/моль |
| Зовнішній вигляд | Білі напівпрозорі кристали |
| Густина | 1,473 g cm−3 |
| Розчинність (вода) | 18 g L−1 |
| Кислотність (pKa) | 2,201 |
| Основність (pKb) | 11,796 |
| Ізоелектрична точка | 4.75 |
| Показник заломлення (nD) | 1,4936 |
| Дипольний момент | 0,1271305813 D |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 |
-344,9 кДж/моль |
| Ст. ентальпія згоряння ΔcH 298 |
-2,73083 МДж/моль |
| Фармакологія | |
| Період напіввиведення | 20-45 min |
| Шляхи введення | Intramuscular, Oral |
| Небезпеки | |
| Класифікація ЄС | |
| S-фрази | S26, S36 |
| NFPA 704 | |
| Температура спалаху | 193 °C |
| Температура самозаймання | 365 °C |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Історія відкриття
ред.Вперше нікотинову кислоту було отримано дослідником Хубером в 1867 році при окисленні нікотину хромовою кислотою. Сучасна назва нікотинова кислота отримала в 1873 році, коли австрійський хімік Хуго Вайдель синтезував цю речовину, окислюючи нікотин нітратною кислотою. Однак про вітамінні властивості нікотинової кислоти ще нічого не було відомо.
У 1920-х роках американський лікар Джозеф Голдбергер припустив існування вітаміну РР, що сприяє профілактиці і лікуванню пелагри. І тільки в 1937 році групою вчених на чолі з Елвейджем було доведено, що нікотинова кислота і є вітамін РР. У 1938 році в СРСР вже успішно лікували пелагру нікотиновою кислотою у таборах НКВД.
Фармакологічна дія
ред.В організмі людини нікотинова кислота перетворюється в нікотинамід, який зв'язується з коензимами кодегидрогенази I і II (НАД+ і НАДФ+), які переносять водень, бере участь в метаболізмі жирів, протеїнів, амінокислот, пуринів, тканинному диханні, глікогенолізі, синтетичних процесах.
Нікотинова кислота, нікотинамід та ніацин являють собою різні хімічні сполуки, однак вони є єдиними ланцюгом біохімічного перетворення вітаміну в організмі. Отже у більшості випадків їх називають, як синоніми вітаміну В3.
Нестача цього вітаміну призводить до дерматизму, деменції, діареї, а також спричинює таке захворювання як пелагра (авітамінозне захворювання з переважним ураженням шкіри). За структурою нікотинова кислота є похідним гетероциклічної сполуки піридину. Вітамін B3 у значних кількостях знаходиться у житньому хлібі, гречці, квасолі, м'ясі, печінці, нирках. Добова норма для дорослої людини приблизно 25 мг.[3]
Всмоктується вітамін B3 у тонкій кишці простою дифузією. З ентероцитів він потрапляє в кров, якою переноситься в печінку та інші органи. У клітинах нікотинова кислота перетворюється в НАД+ і НАДФ+. Біосинтез НАД+ із нікотинаміду здійснюється таким методом:[3]
- нікотинамід + фосфорибозилпірофосфат → нікотинамід-мононуклеотид + Н4Р2О7;
- нікотинамід-мононуклеотид + АТФ → НАД+ + пірофосфат.
Процес утворення НАД+ здійснюється під впливом специфічних пірофосфорилаз, розміщених як у цитоплазмі, так і в мітохондріях.
НАДФ утворюється в цитоплазмі з НАД+ за допомогою специфічної кінази: НАД+ + АТФ → НАДФ+ + АДФ.
НАД+ і НАДФ виявлені в усіх типах клітин. У клітинах печінки приблизно 60 % усього вмісту НАД+ знаходиться в мітохондріях, а 40 % — у цитоплазмі. В окисненому стані НАД+ має вузьку смугу поглинання в ультрафіолетовій частині спектра з максимумом на довжині хвилі 260 нм. У відновленому стані виникає друга смуга при 340 нм, при одночасному зменшенні інтенсивності смуги при 260 нм. Окиснені форми НАД+ і НАДФ+ проявляють виражену флюорисценцію з довжиною хвилі 440 нм.[3]
Біологічні функції
ред.У складі НАД+ і НАДФ+ ніацин бере участь в обміні речовин. Є приблизно сотня нікотинамідзалежних ферментів. НАД+ і НАДФ+ є коферментами багатьох дегідрогеназ, необхідних для вироблення енергії в клітині: виступають акцепторами і проміжними переносниками атомів водню на початкових стадіях окиснення вуглеводів, жирних кислот, амінокислот, гліцерину, на стадії циклу Кребса і в термінальних стадіях дегідрування в дихальному ланцюзі та монооксигеназному ланцюзі.[3]
Таким чином, вітамін В3 бере участь в енергозабезпеченні клітин і в знешкодженні шляхом окиснення природних та чужорідних речовин (монооксигеназний ланцюг окиснення).
Примітки
ред.- ↑ Niacin. DrugBank: a knowledgebase for drugs, drug actions and drug targets. Архів оригіналу за 25 червня 2013. Процитовано 14-January-2012.
- ↑ Niacin — PubChem Public Chemical Database. The PubChem Project. USA: National Center for Biotechnology Information. Архів оригіналу за 25 червня 2013. Процитовано 29 січня 2013.
- ↑ а б в г Гонський Я. І., Максимчук Т. П. Біохімія людини: підручник. - Тернопіль: Укрмедкнига, 2001. — 736 С. ISBN 966-7364-17-8 (С.130-132)
Джерела
ред.Посилання
ред.- Кислота нікотинова [Архівовано 15 березня 2016 у Wayback Machine.]
