Водневий зв'язок
Водне́вий зв'язо́к — різновид хімічного зв'язку, що реалізується за рахунок електростатичного притягання між воднем (із позитивним частковим зарядом) однієї молекули та атомом з великим значенням електронегативності (О, N, F, а також P[1]) іншої молекули.[2]
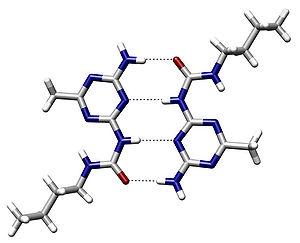

Водневий зв'язок є важливим для органічної хімії. Завдяки водневому зв'язку вода (головний розчинник у неорганічній хімії та біохімії) має високу температуру плавлення і кипіння. Водневий зв'язок з'єднує подвійну спіраль ДНК (носія генетичної інформації), а також відповідає за формування вторинної і третинної структури білків.
Загальний опис
ред.Водневий зв'язок є прикладом трицентрового чотириелектронного зв'язку.
Прослідковується певна аналогія між водневим та ковалентним зв'язком. Зокрема, водневий зв'язок є направленим та насичуваним, що вказує на його резонансну природу (на противагу електростатичній природі йонного зв'язку). Висувається припущення, що йон H+ завдяки своїм унікальним властивостям (він фактично є єдиною частинкою — протоном) виступає аналогом електронної пари в класичному ковалентному зв'язку, тільки з протилежним знаком.
За величиною енергії він на порядок слабший за ковалентний зв'язок. Наприклад, у рідкій воді енергія розриву водневого зв'язку становить 23 кДж/моль, для порівняння енергія розриву ковалентного O—H зв'язку — 470 кДж/моль[3].
Розрізняють міжмолекулярний та внутрішньомолекулярний водневі зв'язки. Часто їх розглядають як частковий випадок координаційного зв'язку, де акцептором електронної пари виступає протонізований значною мірою атом H, що зв'язується з електронегативними атомами N, P, O, S, Hal, відомі також інші водневі зв'язки. Наприклад, C—H…C=C, N—H…N, P—H…P, O—H…O, S—H…S, Hal—H…Hal (галоген). Енергія дисоціації таких зв'язків змінюється в широких межах CH…O чи OH…C=C (2—20 кДж моль−1), OH…O (20—40 кДж моль−1), йонний водневий зв'язок(40—190 кДж моль−1). Типовими довжинами таких зв'язків є: NH…O 1,80 до 2,00 A, OH…O дещо коротший (1,60 до 1,80 A).
В останні роки, крім класичного водневого зв'язку, виділяють слабкий водневий зв'язок, сильний водневий зв'язок та симетричний водневий зв'язок.
Встановлено, що найсильнішим є лінійний водневий зв'язок — атом H та обидва акцепторні атоми знаходяться на одній лінії.
Із встановленням наявності водневого зв'язку в структурі речовини пов'язані певні труднощі, оскільки атом водню важко локалізувати за допомогою стандартного рентгеноструктурного аналізу через його надзвичайно малу відносну масу. Існує кілька критеріїв встановлення водневого зв'язку:
- структурний (за скороченими відстанями між електронегативними атомами та характерними валентними кутами);
- спектроскопічний (за низькочастотним зсувом та уширенням смуг поглинання в ІЧ спектрах, що відповідають зв'язкам E-H; за уширенням піків в 1H ЯМР спектрах).
Асиметричний водневий зв'язок
ред.Водневий зв'язок X…H…Y між атомом H, зв'язаним хімічним зв'язком з електронегативним атомом X, та атомом Y, що є також електронегативним, у випадку, коли віддалі X…H та H…Y є різними. Це зокрема водневі зв'язки у воді, карбонових кислотах.
Внутрішньомолекулярний водневий зв'язок
ред.Водневий зв'язок, в якому атом H є зв'язаним з двома (найчастіше) гетероатомами однієї молекули. У ненасичених системах атом H може замикати 6π-псевдоароматичну електронну оболонку, виступаючи в системі елетронодефіцитним містком — такі ароматичні H-зв'язки особливо стабільні та часто надають речовині особливих властивостей, наприклад, аномальні Стоксові зсуви у люмінофорах.
Міжмолекулярний водневий зв'язок
ред.Водневий зв'язок, в якому атом H зв'язаний з двома (найчастіше) гетероатомами різних молекул. Міцність його залежить від кислотних властивостей протонодонорного й основних властивостей протоноакцепторного атомів.
Див. також
ред.Примітки
ред.- ↑ Møller, Kristian H., Hansen, Anne S., Kjaergaard, Henrik G. Gas Phase Detection of the NH–P Hydrogen Bond and Importance of Secondary Interactions // J. Phys. Chem. A. — 2015. — Т. 119, вип. 44 (13 листопада). — С. 10988–10998. — DOI:. (англ.)
- ↑ Pure and Applied Chemistry. Т. 56, № 11. 1 січня 1984. с. iv. doi:10.1351/pac19845611iv. ISSN 1365-3075 http://dx.doi.org/10.1351/pac19845611iv. Процитовано 26 грудня 2021.
{{cite news}}: Пропущений або порожній|title=(довідка) - ↑ Nelson D.L., Cox M.M. (2008). Lehninger Principles of Biochemistry (вид. 5th). W. H. Freeman. с. 44. ISBN 978-0-7167-7108-1.
Джерела
ред.- Глосарій термінів з хімії / укладачі: Й. Опейда, О. Швайка ; Ін-т фізико-органічної хімії та вуглехімії ім. Л. М. Литвиненка НАН України, Донецький національний університет. — Донецьк : Вебер, 2008. — 738 с. — ISBN 978-966-335-206-0.
| Це незавершена стаття з хімії. Ви можете допомогти проєкту, виправивши або дописавши її. |