Бензидамін
Бензидамін (також відомий як Tantum Verde і під торговою маркою в деяких країнах Maxtra Gargle, Difflam і Septabene), доступний як гідрохлоридна сіль, є місцевою дієюнестероїдного протизапального препарату (НПЗЗ) з місцевими анестетичними та знеболювальними властивостями для полегшення болю та протизапального лікування запальних станів порожнини рота та горла.[1] Він належить до класу хімічних речовин, відомих як індазол.
| |
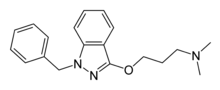
| Систематична назва (IUPAC) | |
| 3-(1-benzyl-1H-indazol-3-yloxy)-N,N-dimethylpropan-1-amine | |
| Ідентифікатори | |
| Номер CAS | |
| Код ATC | |
| PubChem | |
| Хімічні дані | |
| Формула | C19H23N3O |
| Мол. маса | 309,405 г/моль |
| SMILES | & |
| Фармакокінетичні дані | |
| Біодоступність | ? |
| Зв'язування | <20 % |
| Метаболізм | ? |
| Період напіврозпаду | 13 годин |
| Виділення | нирки |
| Терапевтичні застереження | |
| Кат. вагітності |
B2(AU) |
| Лег. статус |
OTC(UK) |
| Шляхи введення | орально, місцево |
Історія ред.
Він був синтезований в Італії в 1964 році та вийшов на ринок в 1966 році[2]
Використання ред.
Медичний ред.
- Одонтостоматологія : гінгівіт, стоматит, глосит, афти, стоматологічні операції та виразки порожнини рота внаслідок променевої терапії.
- Оториноларингологія: залозиста лихоманка, фарингіт, тонзиліт, мукозит після тонзилектомії, променевий або інтубаційний.
Його можна застосовувати окремо або як доповнення до іншої терапії, що дає можливість підвищення терапевтичного ефекту з невеликим ризиком взаємодії.
На деяких ринках препарат поставляється у вигляді безрецептурного крему (Lonol у Мексиці від Boehringer Ingelheim), що застосовується для місцевого лікування захворювань опорно-рухового апарату: розтягнень, розтягнень, бурситу, тендиніту, синовіту, міалгії, періартриту.
Рекреаційний ред.
Бензидамін використовується в рекреаційних цілях. При передозуванні діє як деліріант і стимулятор ЦНС.[3] Про таке використання, особливо серед підлітків, було зареєстровано в Бразилії,[4][5] Польщі,[3] Румунії та Туреччині.
Протипоказання ред.
Протипоказань до застосування бензидаміну немає, за винятком відомої гіперчутливості.
Побічні ефекти ред.
Бензидамін переноситься добре. Іноді можуть виникати оніміння тканин ротової порожнини або відчуття печіння, а також свербіж, шкірний висип, набряк або почервоніння шкіри, утруднене дихання та хрипи.
Фармакологія ред.
Він вибірково зв'язується із запаленими тканинами (інгібітор простагландинсинтетази) і, як правило, не має побічних системних ефектів. На відміну від інших НПЗЗ, він не пригнічує циклооксигеназу або ліпооксигеназу і не є ульцерогенним.[3][6] Він має потужний зміцнюючий ефект і має перехресну сенсибілізацію з наркотиками, такими як героїн і кокаїн у тварин. Передбачається, що він має агоністичну дію на канабіноїди.[7]
Фармакокінетика ред.
Бензидамін погано всмоктується через шкіру[8] та інтравагінально.[9]
Синтез ред.
Синтез починається з реакції N -бензильного похідного з метилантранілату з азотистою кислотою з утворенням N -нітрозопохідного. Відновлення за допомогою тіосульфату натрію призводить до тимчасового гідразину (3), який зазнає спонтанного внутрішнього утворення гідразиду. Обробка еноляту цього аміду 3-хлор-1-диметиламінопропаном дає бензидамін (5). Будь ласка, зверніть увагу, що в цьому розділі є помилка: US3318905 стверджує, що нітрозопохідне відновлюється гідросульфітом натрію (дітіонітом натрію), а не гіпосульфітом натрію (тіосульфатом натрію), як показано на схемі вище та вказано в тексті.
Цікавий альтернативний синтез цієї речовини починається шляхом послідовної реакції N -бензиланіліну з фосгеном, а потім з азидом натрію з утворенням відповідного карбонілазиду. При нагріванні виділяється азот, і в результаті утворюється роздільна суміш продукту введення нітрену та бажаного кетоїндазолу. Остання реакція є продуктом типу перегрупування Курціуса з утворенням N-ізоціаната #, який потім циклізується. Алкілування енолу метоксидом натрію та 3-диметиламінопропілхлоридом дає бензидамін.
Альтернативно, використання хлорацетаміду на стадії алкілування з подальшим кислотним гідролізом дає натомість бендазак.
Дослідження ред.
Дослідження показують, що бензидамін має помітну антибактеріальну активність in vitro, а також проявляється синергізм у поєднанні з іншими антибіотиками, особливо тетрациклінами, проти стійких до антибіотиків штамів Золотистого стафілокока та Синьогнійної палички.[12][13]
Він також має деяку канабіноїдну активність у щурів, але не був протестований на людях.[7] Також передбачається, що він діє на рецептори 5-HT2A через його структурну схожість із серотоніном.[2]
Див. також ред.
Примітки ред.
- ↑ Turnbull RS (February 1995). Benzydamine Hydrochloride (Tantum) in the management of oral inflammatory conditions. Journal. 61 (2): 127—34. PMID 7600413.
- ↑ а б DEXTROMETHORPHAN AND BENZYDAMINE'S USE AND MISUSE. Flipper.diff.org. Процитовано 25 червня 2022.
- ↑ а б в Anand JS, Glebocka ML, Korolkiewicz RP (2007). Recreational abuse with benzydamine hydrochloride (tantum rosa). Clinical Toxicology. 45 (2): 198—9. doi:10.1080/15563650600981210. PMID 17364645.
- ↑ Opaleye ES, Noto AR, Sanchez Z, Moura YG, Galduróz JC, Carlini EA (September 2009). Recreational use of benzydamine as a hallucinogen among street youth in Brazil. Revista Brasileira de Psiquiatria. 31 (3): 208—13. doi:10.1590/S1516-44462009000300005. PMID 19784487.
- ↑ Mota DM, Costa AA, Teixeira C, Bastos AA, Dias MF (May 2010). Use abusive of benzydamine in Brazil: an overview in pharmacovigilance. Ciencia & Saude Coletiva (порт.). 15 (3): 717—24. doi:10.1590/S1413-81232010000300014. PMID 20464184.
- ↑ Müller-Peddinghaus R (May 1987). New pharmacologic and biochemical findings on the mechanism of action of the non-steroidal antiphlogistic, benzydamine. A synopsis. Arzneimittel-Forschung (German) . 37 (5A): 635—45. PMID 3304305.
- ↑ а б Avvisati R, Meringolo M, Stendardo E, Malavasi E, Marinelli S, Badiani A (March 2018). Intravenous self-administration of benzydamine, a non-steroidal anti-inflammatory drug with a central cannabinoidergic mechanism of action (PDF). Addiction Biology. 23 (2): 610—619. doi:10.1111/adb.12516. PMID 28429885.
- ↑ Baldock GA, Brodie RR, Chasseaud LF, Taylor T, Walmsley LM, Catanese B (October 1991). Pharmacokinetics of benzydamine after intravenous, oral, and topical doses to human subjects. Biopharmaceutics & Drug Disposition. 12 (7): 481—92. doi:10.1002/bdd.2510120702. PMID 1932611.
- ↑ Maamer M, Aurousseau M, Colau JC (1987). Concentration of benzydamine in vaginal mucosa following local application: an experimental and clinical study. International Journal of Tissue Reactions. 9 (2): 135—45. PMID 3610512.
- ↑ а б Palazzo G, Corsi G, Baiocchi L, Silvestrini B (January 1966). Synthesis and pharmacological properties of 1-substituted 3-dimethylaminoalkoxy-1H-indazoles. Journal of Medicinal Chemistry. 9 (1): 38—41. doi:10.1021/jm00319a009. PMID 5958958.
- ↑ Baiocchi L, Corsi G, Palazzo G (1965). Ricerche nel campo degli indazoli.—Nota 1. Sulla ciclizzazione termica di azidi di acidi N-aril-N-benzil-carbamici. Annali di Chimica. 55: 116—25.
- ↑ Fanaki NH, el-Nakeeb MA (December 1992). Antimicrobial activity of benzydamine, a non-steroid anti-inflammatory agent. Journal of Chemotherapy. 4 (6): 347—52. doi:10.1080/1120009X.1992.11739190. PMID 1287137.
- ↑ Fanaki NH, El-Nakeeb MA (March 1996). Antibacterial activity of benzydamine and antibiotic-benzydamine combinations against multifold resistant clinical isolates. Arzneimittel-Forschung. 46 (3): 320—3. PMID 8901158.
Посилання ред.
- Benzydamine oral rinse. Medicinenet.
- Difflam spray (benzydamine). Net Doctor, UK. 8 березня 2020.
- Tantum Verde (benzydamine). Carysfort Healthcare Limited, Ireland. Архів оригіналу за 25 листопада 2015.