Діоксид кремнію
Діокси́д кре́мнію (кремнезем, SiO2) (англ. silica, нім. Siliziumdioxid n) — сполука ковалентної природи.
| Діоксид кремнію | |
 | |
| Маса | 1,0E−25 кг[1] |
|---|---|
| Хімічна формула | SiO₂[1] |
| Канонічна формула SMILES | O=[Si]=O[1] |
| Температура плавлення | 3110 ± 1 ℉[2] |
| Точка кипіння | 4046 ± 1 ℉ |
| Тиск насиченої пари | 0 ± 1 mm Hg |
| Розчинність | 0,12 g/dm³[3] і 0,9 g/dm³[4] |
| Класифікація та маркування безпеки | NFPA 704: Standard System for the Identification of the Hazards of Materials for Emergency Response[d] |
| Наявний у таксона | G. wallichiid[5], P. edulis[6], S. elongatusd[5], E. telmateia[7] і E. arvense[7] |
| Ідентифікатор NCI Thesaurus | C29853[8] |
| | |


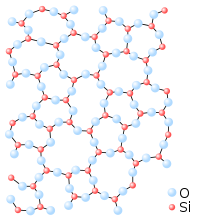
Загальний опис
ред.Найвідоміший мінерал — кварц, що має вигляд безбарвних кристалів із tпл 1713–1728 °C та високою твердістю і міцністю. При високих температурах діоксид кремнію існує в молекулярному вигляді. Молекула SiO2 має лінійну форму, довжини зв'язків Si-O 1.495 Å. Є надзичайно реакційноздатною, тому зафіксована лише спектроскопічно. Втім, методами матричної ізоляції зафіксовано димер (SiO2)2 та тример (SiO2)3, що мають, відповідно, симетрії D2h та D3h.
Кремнезем — один з найважливіших і найпоширеніших мінералів кремнію. Формула: SiO2. У природі буває у вигляді кварцу, гірського кришталю тощо. Крім того під терміном кремнезем часто розуміють будь-яку поліморфну модифікацію діоксиду кремнію.
Діоксид кремнію зустрічається в природі головним чином у вигляді мінералу кварцу. Це дуже тверда речовина з температурою плавлення 1728 °С. Великі прозорі і безбарвні кристали природного кварцу називають гірським кришталем. Кварц входить до складу багатьох гірських порід, наприклад граніту, гнейсу тощо. Звичайний пісок складається з дрібненьких кристалітів кремнезему. Пісок, що складається з чистого кварцового скла, зветься кварцовим і використовується в промисловості, зокрема, для добування металічного кремнію. У чистому вигляді пісок має білий колір, але здебільшого він буває забарвлений домішками сполук заліза в жовтуватий колір.
Інколи діоксид кремнію зустрічається в природі в аморфному стані. Таку речовину називають трепелом, або інфузорною землею. Місцями трепел утворює значні поклади, які виникли з залишків деяких водоростей, до складу яких входить діоксид кремнію.
У хімічному відношенні діоксид кремнію є кислотним оксидом — ангідридом силікатної кислоти H2SiO3. Однак з водою SiO2 безпосередньо не взаємодіє, тому силікатну кислоту можна одержати лише посереднім шляхом. Кислоти на SiO2 теж не діють, за винятком фторидної кислоти, яка дуже енергійно реагує з ним:
- SiO2 + 4HF = SiF4↑ + 2H2O
З основними оксидами і твердими лугами при високій температурі SiO2 утворює солі, які називають силікатами, наприклад:
- SiO2 + CaO = CaSiO3
Здатен відновлюватись до моноксиду кремнію при взаємодії з вугіллям чи чистим кремнієм:
- SiO2 + C = SiO + CO
Використання
ред.Діоксид кремнію є природним ізолятором у кремнієвій мікроелектроніці. Тонка плівка діоксиду кремнію утворюється на поверхні напівпровідника при контакті з повітрям і створює необхідні для транзисторів діелектричні шари.
Аморфний непористий діоксид кремнію застосовується в харчовій промисловості як допоміжна речовина E551, що перешкоджає злежуванню та грудкуванню, парафармацевтиці (зубні пасти), у фармацевтичній промисловості як допоміжна речовина (внесений до більшості фармакопей), а також дієтична добавка або лікарський препарат як ентеросорбент[9].
Див. також
ред.Примітки
ред.- ↑ а б в Silica
- ↑ Silica, amorphous — Центри з контролю та профілактики захворювань в США.
- ↑ https://www.lenntech.com/periodic/water/silicon/silicon-and-water.htm
- ↑ http://www.minsocam.org/ammin/AM62/AM62_1052.pdf
- ↑ а б Teaford M. F. Significance of silica in leaves to long-tailed macaques (Macaca fascicularis), Significance of Silica in Leaves to Long-Tailed Macaques (Macaca fascicularis) // Folia Primatologica — Karger Publishers, Brill, 1995. — Vol. 64, Iss. 1-2. — P. 30–36. — ISSN 0015-5713; 1421-9980 — doi:10.1159/000156829
- ↑ Lux A., Luxová M., Abe J. та ін. Silicification of bamboo (Phyllostachys heterocycla Mitf.) root and leaf — 2013. — С. 85–91. — doi:10.1007/978-94-017-2923-9_9
- ↑ а б N. Ghassemi, A. Ghanadi A Study on the Morphology and Phytochemlstry of Some Iranian Equisetum Species // Planta Med. — Thieme Medical Publishers (Germany), 2007. — Vol. 59, Iss. S 1. — P. A638–A638. — ISSN 0032-0943; 1439-0221 — doi:10.1055/S-2006-959880
- ↑ Global Substance Registration System
- ↑ Энтеросорбенты: против отравлений. «Фармацевтический вестник» № 8 (668) Март 06, 2012 г.
Джерела
ред.- Деркач Ф. А. Хімія. — Львів : Львівський університет, 1968. — 312 с.
- Мала гірнича енциклопедія : у 3 т. / за ред. В. С. Білецького. — Д. : Донбас, 2004. — Т. 1 : А — К. — 640 с. — ISBN 966-7804-14-3.
Інтернет-ресурси
ред.- Formation of silicon oxide layers in the semiconductor industry [Архівовано 14 лютого 2008 у Wayback Machine.]. LPCVD and PECVD method in comparison. Stress prevention.
- Quartz SiO2 piezoelectric properties
- Silica (SiO2) and Water [Архівовано 7 червня 2010 у Wayback Machine.]
- Epidemiological evidence on the carcinogenicity of silica: factors in scientific judgement by C. Soutar and others. Institute of Occupational Medicine Research Report TM/97/09
- Scientific opinion on the health effects of airborne silica by A Pilkington and others. Institute of Occupational Medicine Research Report TM/95/08