Борна кислота
Бо́рна кислота́ (лат. acidum boricum, о́ртобо́рна, о́ртобора́тна, бора́тна кислота́) Н3ВО3[1], B(OH)3 — це слабка неорганічна кислота. Виглядає як лускаті, безбарвні, жирні на дотик кристали малорозчинні у воді при кімнатній температурі і значно більше розчинні у гарячій воді.
| Борна кислота | |
|---|---|
 Структурна формула
| |
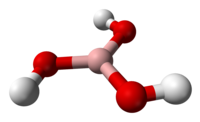
| |
 Кристали борної кислоти
| |
| Назва за IUPAC | Борна кислота |
| Ідентифікатори | |
| Номер CAS | 10043-35-3 |
| PubChem | 7628 |
| Номер EINECS | 233-139-2 |
| DrugBank | 11326 |
| KEGG | D01089 |
| ChEBI | 33118 |
| RTECS | ED4550000 |
| Код ATC | S02AA03 і D08AD |
| SMILES | B(O)(O)O |
| InChI | 1/BH3O3/c2-1(3)4/h2-4H |
| Номер Гмеліна | 1585 |
| Властивості | |
| Молекулярна формула | H3BO3 |
| Молярна маса | 61,83 г/моль |
| Зовнішній вигляд | Біла кристалічна речовина |
| Густина | 1,435 г/см3 |
| Тпл | 170,9 °C |
| Ткип | 300 °C |
| Розчинність (вода) | 2,52 г/100 мл (0 °C) 4,72 г/100 мл (20 °C) 5,7 г/100 мл (25 °C) 19,10 г/100 мл (80 °C) 27,53 г/100 мл (100 °C) |
| Кислотність (pKa) | 9,24 |
| Структура | |
| Геометрія | Рівносторонній трикутник |
| Небезпеки | |
| ЛД50 | 2660 мг/кг, орально (криса) |
| Класифікація ЄС | |
| R-фрази | R60 R61 |
| S-фрази | S53 S45 |
| NFPA 704 | |
| Температура спалаху | не запалюється |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Термін «борна кислота» також використовується для будь-якої оксокислоти бору, такий як метаборна кислота HBO2 і тетраборна кислота H2B4O7.
Поширення у природі ред.
На незв'язану кислоту можна натрапити в деяких вулканічних місцевостях таких, як Тоскана, Ліпарські острови і Невада. Її також можна виявити в складі багатьох мінералів (бура, борацит і колеманіт). Наявність борної кислоти та її солей знайдено в морській воді. Вона також є в рослинах і майже у всіх овочах (яблука, сливи, груші і т. д.).
Фізичні властивості ред.
Кристали білого кольору або безбарвні, блискучі, жирні на дотик пластинки. Розчинна у воді та 96 % спирті, легкорозчинна у киплячій воді і гліцерині — 85 %.[1] Водні розчини борної кислоти є сумішшю поліборних кислот загальної формули Н3m-2nВmО3m-n. У природі зустрічається у вигляді мінералу сасоліну.
Відстань між сусідніми шарами — 318 пм.
Хімічні властивості ред.
Борна кислота виявляє дуже слабкі кислотні властивості. Вона порівняно мало розчинна у воді. Її кислотні властивості обумовлені не відщепленням катіона Н+, а приєднанням гідроксильного аніона (поведінка характерна кислотам Льюїса):
- Н3ВО3 + Н2О ⇄ Н[B(OH)4]: Н[B(OH)4] ⇄ [B(OH)4]- + H+
- Ka = 5,8⋅10−10 моль/л; pKa = 9,24.
Також особливістю борної кислоти є те, що при збільшенні її концентрації вище 0,1 моль/л зростає її сила у зв'язку з утворенням поліборних кислот[2]:
3B(OH)3 = B3O3(OH)4- + H+ + 2H2O
5B(OH)3 = B5O6(OH)4- + H+ + 5H2O
Вона легко витісняється із розчинів своїх солей більшістю інших кислот. Її солі, борати, отримуються зазвичай від різних поліборних кислот, найчастіше тетраборної H2B4O7, яка є значно сильнішою кислотою, ніж ортоборна.
Дуже слабкі ознаки амфотерності B(OH)3 проявлює, утворюючи малостійкий гідросульфат бору В(HSO4)3.
При нейтралізації ортоборної кислоти лугами, у водних розчинах, не утворюються сполуки, що містять іон (ВО3)3−, оскільки ортоборати гідролізуються практично повністю, внаслідок занадто малої константи утворення [В(ОН)4]− — утворюються тетраборати, метаборати або солі інших поліборних кислот:
- 4H3BO3 + 2NaOH → Na2B4O7 + 7H2O
Надлишком лугу тетраборати можуть бути переведені в метаборати:
- H3BO3 + NaOH → NaBO2 + 2H2O
Піроліз ред.
При нагріванні ортоборної кислоти вище 140 °С втрачає воду і переходить у метаборну кислоту.[3][4]
B(OH)3 → HBO2 + H2O
Потім, при нагріванні вище 180 °С у тетраборну.
4HBO2 → H2B4O7 + H2O
При подальшому нагріванні до 530 °C зневоднюється до борного ангідриду (B2O3). Однак повної дегідратації досягти дуже важко, навіть при температурі 500 °С у розплаві міститься 5 % води.[2]
H2B4O7 → 2B2O3 + H2O
Естерифікація ред.
Борна кислота естерифікується, в присутності концентрованої сульфатної кислоти, зі спиртами утворюючи естери борної кислоти B(OR)3, де R це алкільна або арильна група.[5]
B(OH)3 + 3ROH → B(OR)3 + 3H2O
Утворення брометилового естеру В(ОСН3)3 являє собою якісну реакцію на Н3ВО3 та солі борних кислот. При підпалюванні борний естер горить яскраво-зеленим полум'ям.[6]
Взаємодія з металами та їх оксидами ред.
При нагріванні борна кислота розчиняє оксиди металів, утворюючи солі: При надлишку оксиду утворюється метаборат кальцію:
2H3BO3 + CaO → Ca(BO2)2 + 3H2O
При нестачі оксиду утворюється тетраборат кальцію:
4H3BO3 + CaO → CaB4O7 + 6H2O
Взаємодіє з металами при нагріванні:
2Na + 2H3BO3 → NaBO2 + 2H2O + H2
Отримання ред.
Борна кислота була вперше виготовлена Вільгельмом Гомбергом[en] (1652–1715) з бури, під дією неорганічних кислот, і він назвав її sal sedativum Hombergi («заспокійлива сіль Хомберга»).
- Na2B4O7·10H2O + 2 HCl → 4 B(OH)3 (або H3BO3) + 2 NaCl + 5 H2O
Застосування ред.
Борну кислоту широко використовують в медицині як слабкий антисептичний засіб: у вигляді 1–2 %-вого водного розчину — для промивання ран та слизових оболонок статевих органів; у порошку — для лікування носа й вуха; у спиртових розчинах і мазях — для лікування шкіри. Крім того, борну кислоту застосовують для дублення шкіри, у виробництві скла, виготовленні деяких фарб та емалей.
Використання в ядерних реакторах ред.
Борну кислоту у вигляді водного розчину використовують у ядерних реакторах з водою під тиском (водно-водяні реактори). У цьому типі реакторів водний розчин борної кислоти використовують, як поглинач нейтронів внаслідок вмісту у кислоті елементу бору. У природі елемент бор має два ізотопи — 10В (20 % вмісту) та 11В (80 % вмісту). Для поглинання нейтронів потрібен високий абсорбційний коефіцієнт і тому, як поглинач нейтронів краще використовувати ізотоп 10В для управління ядерною реакцією та її потужністю у реакторі. При цьому проходять наступні ядерні перетворення (реакції):
Примітки ред.
- ↑ а б П. О. Безуглий, 2008, С.100
- ↑ а б Ткачев К. В., Плышевский Ю. С., 1983, С.19-20
- ↑ Kaur, Gurwinder; Kainth, Shagun; Kumar, Rohit; Sharma, Piyush; Pandey, O. P. (2021-10). Reaction kinetics during non-isothermal solid-state synthesis of boron trioxide via boric acid dehydration. Reaction Kinetics, Mechanisms and Catalysis (англ.). Т. 134, № 1. с. 347—359. doi:10.1007/s11144-021-02084-8. ISSN 1878-5190. Процитовано 31 травня 2023.
- ↑ Aghili, Siavash; Panjepour, Masoud; Meratian, Mahmood (2018-03). Kinetic analysis of formation of boron trioxide from thermal decomposition of boric acid under non-isothermal conditions. Journal of Thermal Analysis and Calorimetry (англ.). Т. 131, № 3. с. 2443—2455. doi:10.1007/s10973-017-6740-3. ISSN 1388-6150. Процитовано 31 травня 2023.
- ↑ Brown, Herbert C.; Mead, Edward J.; Shoaf, Charles J. (1956-08). Convenient Procedures for the Preparation of Alkyl Borate Esters 1-3. Journal of the American Chemical Society (англ.). Т. 78, № 15. с. 3613—3614. doi:10.1021/ja01596a015. ISSN 0002-7863. Процитовано 31 травня 2023.
- ↑ Кійко С. М., Ніколайчук О. Г., Уржунцева В. В. (2012). Лабораторний практикум з неорганічного синтезу: навчальний посібник. Харків: ХНУ імені В. Н. Каразіна. с. 56—57.
Джерела ред.
- Фармацевтична хімія : [арх. 11 березня 2021] : підручник / ред. П. О. Безуглий. — Вінниця : Нова Книга, 2008. — С. 100—102. — 560 с. — ISBN 978-966-382-113-9.
- Ткачев К. В., Плышевский Ю. С. (1983). Технология неорганических соединений бора. Л: Химия. с. 19–20 (рос.)
- Українська радянська енциклопедія : у 12 т. / гол. ред. М. П. Бажан ; редкол.: О. К. Антонов та ін. — 2-ге вид. — К. : Головна редакція УРЕ, 1974–1985. — [сторінка?]
Література ред.
- Фармакологія: підручник (ВНЗ І—ІІІ р. а.) / І. В. Нековаль, Т. В. Казанюк. — 7-е вид., переробл. і допов. — «Медицина», 2016 — 552 с. ISBN 978-617-505-507-6. — [сторінка?]
Посилання ред.
- КИСЛОТА БОРНА [Архівовано 9 червня 2016 у Wayback Machine.] //Фармацевтична енциклопедія
| Це незавершена стаття про неорганічну сполуку. Ви можете допомогти проєкту, виправивши або дописавши її. |
