Ізобутанол
Ізобутанол (номенклатура IUPAC: 2-метилпропан-1-ол) це органічна сполука з формулою (CH3)2CHCH2OH. Ця безбарвна, легкозаймиста рідина з характерним запахом, використовується в основному як розчинник. Його ізомери, інші бутаноли, включають n - бутанол, 2-бутанол і трет-Бутанол. Всі вони мають промислове значення.
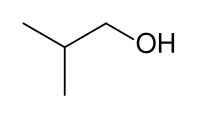
| 2-метилпропан-1-ол | |
|---|---|
| |

| |
| Систематична назва | 2-метилпропан-1-ол |
| Інші назви | Ізобутанол |
| Ідентифікатори | |
| Номер CAS | 78-83-1 |
| Номер EINECS | 201-148-0 |
| KEGG | C14710 |
| ChEBI | 46645 |
| RTECS | NP9625000 |
| SMILES | CC(C)CO[1] |
| InChI | InChI=1S/C4H10O/c1-4(2)3-5/h4-5H,3H2,1-2H3 |
| Номер Бельштейна | 1730878 |
| Номер Гмеліна | 49282 |
| Властивості | |
| Молекулярна формула | C4H10O |
| Молярна маса | 74,12 г/моль |
| Зовнішній вигляд | безбарвна рідина |
| Густина | 0,8016 г/см3 |
| Тпл | -108 |
| Ткип | 107,89 |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Виробництво
ред.Промислове отримання ізобутанолу зводиться до використання трьох основних методів:
- Карбонілювання пропену (оксосинтез),
- Каталітичне гідрування оксиду вуглецю (II),
- Реакції гомологізації [2].
Перший метод ґрунтується на реакції пропілену з монооксидом вуглецю і гідрогеном в присутності кобальтового каталізатору при температурі 100-180 °C і тиску 20-30·106 Па. При цьому в якості продуктів одночасно утворюється бутаналь та ізобутаналь, співвідношення яких в даних умовах становить 3:1. Сучасні процеси, в яких застосовується каталізатор на основі модифікованого родію, мають велику селективність, даючи 92-95% бутаналю. У той же час використання немодифікованого родію призводить до 50% вмісту ізобутаналю в кінцевій суміші продуктів. Подальше гідрування ізобутаналю дає ізобутіловий спирт [2].
Ізобутанол може бути також отриманий реакцією пропілену з монооксидом вуглецю і води. Даний процес був розроблений Реппе в 1942 році. В ході цієї реакції спирт утворюється безпосередньо з алкену, проте, як і в разі першого методу, утворюється суміш двох ізомерних спиртів [2].
Компанія BASF розробила спосіб отримання ізобутилового спирту, заснований на каталітичному гідруванні монооксиду вуглецю і призводить до утворення суміші, що містить 50% метанолу і 11-14% ізобутанолу, а також інші продукти. BASF припинила виробляти ізобутиловий спирт цим методом після розробки оксосінтезу і нафтохімічного шляху синтезу ізобутанолу [2].
Фізичні властивості
ред.Ізобутиловий спирт - це безбарвна горюча рідина з характерним запахом. Він змішується з більшістю органічних розчинників. Його розчинність в воді становить 8,5% мас. при 20 °C; 7,5% мас. при 30 °C, тоді як концентрація насиченого розчину води в ізобутиловому спирті становить 15% мас. при 20 °C і 17,3% мас. при 30 °C. Ізобутиловий спирт утворює азеотропні суміші з водою і толуеном, що містять 67-70% і 44,5% ізобутилового спирту і киплячі при 89,8 °C і 101,2 °C відповідно [2].
Хімічні властивості
ред.Дегідратація ізобутилового спирту проводиться в промислових масштабах. Її проводять у присутності γ-оксиду алюмінію при 300-350 °C з практично повною конверсією і виходом ізобутилену більше 90%. Ізобутиловий спирт може бути дегідрований в присутності оксиду марганцю(IV) MnO2, оксиду селену(IV) SeO2 і навіть у відсутності окислювачів. Він перетворюється в ізомасляну кислоту під дією стандартних окислювачів. У присутності кислотних каталізаторів ізобутанол може утворювати складні ефіри з карбоновими кислотами [2].
Застосування
ред.Ізобутиловий спирт застосовується в різних областях і, завдяки низькій вартості, може служити заміною бутанолу-1. Він використовується в якості розчинника, добавки до нітроцелюлози та гуми, осушувача, компонента чорнила для друку [2].
Безпека
ред.Найнижча опублікована летальна доза для ізобутилового спирту становить 2460 мг/кг (щури, перорально) та 3400 мг/кг (кролики, через шкіру), що свідчить про низьку токсичність при локальній дії. Летальна концентрація становить 1330 мг/л (риби, 96 год.). Наркотична доза для мишей дорівнює 6400 м.ч. протягом 136 год. Ізобутиловий спирт викликає подразнення слизової очей і шкірних покривів у кроликів. Дослідження показали, що ізобутіловий спирт може мати канцерогенну дію [2].