Хвороба Гантінгтона
Хворо́ба Га́нтінгтона (відома також як Хорéя Га́нтінгтона)— генетичне захворювання нервової системи, що уражає людину у віці 35-50 років внаслідок змін у гені IT-15, що знаходиться на 4-ій хромосомі, яке призводить до атрофії стріатума, а на пізній стадії — до атрофії кори головного мозку. З моменту появи перших симптомів тривалість життя становить близько 15-20 років. Смерть зазвичай настає не через саму хворобу Гантінгтона, а внаслідок її ускладнень.
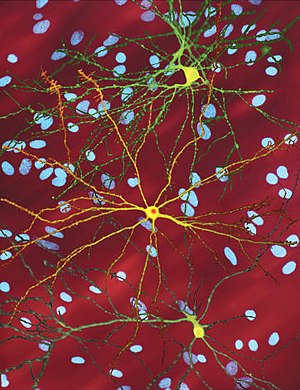
| Хвороба Гантінгтона | |
|---|---|
 | |
| Спеціальність | неврологія |
| Симптоми | зміна особистостіd, хорея, схуднення і деменція |
| Причини | trinucleotide repeat expansiond |
| Метод діагностики | genetic testingd |
| Препарати | пімозид[1], баклофен[1], Перфеназин[1], убіхінон[1], Тетрабеназин[2] і Тетрабеназин[3] |
| Частота | 0.0123% (Велика Британія) |
| Класифікація та зовнішні ресурси | |
| МКХ-11 | 8A01.10 |
| МКХ-10 | G10, F02.2 |
| OMIM | 143100 |
| DiseasesDB | 6060 |
| MedlinePlus | 000770 |
| eMedicine | article/1150165 article/792600 |
| MeSH | D006816 |
| | |
Етіологія ред.
Захворювання спричинює дуплікація кодона CAG у гені IT-15. Цей ген кодує 350-kDa білок гантінгтін із невідомою функцією. Ген дикого типу (не мутантного) у різних людей демонструє різну кількість CAG-повторів, хвороба ж розвивається тоді, коли їх число перевищує 36. При цьому відомо, що захворювання завжди настає, коли кількість CAG-повторів 40 і більше (100 % пенетрантність). При кількості CAG-повторів 36-39 захворювання проявляється у більш пізньому віці і у легшій формі.
Мутантний ген домінує над здоровим. Тому, відповідно до аутосомно-домінантного типу успадкування, діти пацієнтів із хворобою Гантінгтона в 50 % випадків не успадковують дефектного гена.
Гантінгтон-ген мають усі здорові люди, при цьому кількість CAG-повторів у ньому може варіювати. У нормі вона становить 15-27 CAG-повторів. Коли CAG-повторів 28 і більше є ризик, що з кожним поколінням їхня кількість буде збільшуватись. Цим пояснюється виникнення хвороби в сім'ях, де не було хворих у родоводі.
При успадкуванні гену від батька ризик збільшення кількості CAG-повторів є більшим ніж при успадкуванні від матері. Це пов'язано з нестабільністю гена при сперматогенезі.
Мутантний ген був виявлений у 1993 році.
Патогенез ред.
Науковці довгий час намагалися зрозуміти, чому токсичний білок, що виробляється геном, зустрічається в усіх клітинах організму, але пошкоджує тільки нейрони, причому переважно в смугастому тілі — області мозку, що контролює рух. Один із механізмів було виявлено під час досліджень, результати яких показали інший білок під назвою Rhes, який зустрічається тільки в смугастому тілі. Коли Rhes взаємодіє з білком, що виробляються дефектним геном IT-15, утворюється так званий химерний білок SUMO, що власне і спричинює токсичну дію на нейрони.
Науково-дослідна робота ред.
Роль Rhes і химерного продукту експресії IT-15 було підтверджено в експерименті на людських ембріональних клітинах і клітинах мишачого мозку. Кожну колонію клітин дослідники змішали з різними комбінаціями нормального білка, його мутантної версії і білка Rhes. Результат експерименту показав, що смерть клітин настає лише тоді, коли в них одночасно виявляються білок-мутант і Rhes.[4]
На наступному етапі дослідження науковці мали намір з'ясувати, чи може видалення білка Rhes із мозку мишей сповільнити розвиток хвороби Гантінгтона, або запобігти загибелі клітин без негативних побічних ефектів. Якщо експеримент завершиться вдало, можна буде говорити про створення ліків, що блокують Rhes.
Клінічні прояви ред.
Симптоми хвороби Гантінгтона можуть проявитися в будь-якому віці, але частіше це відбувається в 35-44 роки[5][6]. На ранніх стадіях відбуваються невеликі зміни особистості, когнітивних здібностей і фізичних навичок[5]. Зазвичай першими виявляють фізичні симптоми, так як когнітивні та психічні розлади не настільки виражені на ранніх стадіях. Майже у всіх пацієнтів хвороба Гантінгтона в кінцевому підсумку виявляється схожими фізичними симптомами, але початок захворювання, прогресування та ступінь когнітивних і психічних порушень розрізняються в окремих осіб[7][8].
Для початку захворювання найбільш характерна хорея — безладні, неконтрольовані рухи. Хорея на початку може проявлятися у вигляді занепокоєння, невеликих мимовільних або незавершених рухах, порушенні координації і уповільненні стрибкоподібних рухів очей[5].
Неврологічні симптоми захворювання: різкі, раптові рухи, що не піддаються контролю, в інших випадках, навпаки, хворий рухається занадто повільно. Виникають порушення координації рухів, мова стає невиразною. Поступово всі функції, що вимагають м'язового контролю, порушуються: людина починає гримасувати, відчуває проблеми з жуванням і ковтанням. Через швидкий рух очей порушується сон. Зазвичай хворий проходить через всі стадії фізичного розладу, однак вплив хвороби на когнітивні функції у всіх дуже індивідуальний. Найчастіше відбувається розлад абстрактного мислення, людина втрачає здатність до планування власних дій, оцінювання їхньої адекватності. Поступово з'являються проблеми з пам'яттю, може виникнути депресія і паніка, емоційний дефіцит, егоцентризм, агресія, нав'язливі ідеї, проблеми з впізнавання інших людей, гіперсексуальність і посилення шкідливих звичок, таких як алкоголізм чи ігроманія.
| Зауважте, Вікіпедія не дає медичних порад! Якщо у вас виникли проблеми зі здоров'ям — зверніться до лікаря. |
Лікування ред.
Ліків для лікування хвороби Гантінгтона наразі ще не існує, але у цьому напрямку ведеться активна наукова робота. Проте є симптоматичні медичні засоби, завдяки яким можна пригальмувати розвиток деяких симптомів хвороби і покращити якість життя хворих.[9]
Фізичні вправи, спорт та активність дозволяють пацієнтам довше зберігати самостійність, активність, якість життя та навіть зменшувати вираженість хореї.
Застосування тетрабеназину було впроваджено в медичну практику для лікування хореї при хворобі Гантінгтона в 2008 році.[10] Інші медичні засоби, що зменшують прояви хореї — нейролептики та препарати бензодіазепінового ряду.[11] При призначенні таких препаратів необхідно враховувати можливі побічні дії — такі як гіпокінезія, психомоторне сповільнення, сонливість, подовження QT-інтервалу. Важливо не тільки лікувати хорею, але і забезпечити хворому можливість брати участь у його житті настільки, на скільки це можливо і безпечно.
На пізніх стадіях доцільно застосовувати спеціальні меблі — крісла та ліжка, з яких пацієнт не випаде і не пошкодить себе при гіперкінетичних рухах.[12]
Гіпокінезія та ригідність, особливо в ювенільних випадках хвороби, можна лікувати антипаркінсонічними препаратами. Важливо знати, що нейролептики можуть посилювати гіпокінезію та ригідність, тому доречно час від часу переглядати їх необхідність.
Міоклонічну гіперкінезію можна лікувати вальпроєвою кислотою.
Психіатричні симптоми хвороби Гантінгтона такі як депресія, апатія, агресивність, дратівливість, нав'язливість, усуваються препаратами, які використовують для лікування інших психіатричних розладів — наприклад антидепресанти — особливо інгібітори зворотного захвату серотоніну.
Психоз та галюцинації піддаються лікуванню нейролептиками.
Втрата ваги — спостерігається у пацієнтів вже на ранніх стадіях і пов'язана з гіперкінезами та з порушеннями ковтання. Тому рекомендується висококалорійне харчування (5000 ккал на добу), та накладення гастростоми у тих випадках, коли орального харчування не достатньо.
Наразі фірмою Roche проводяться клінічні дослідження нових медикаментів, які дозволять «вимкнути» дефектний ген, що у свою чергу призведе до зменшення патологічного білка гантітгтину. Це так звані анти-сенс-олігонуклеотиди — невеликі молекули, що комплементарно зв'язуються з і-РНК і, таким чином, блокують трансляцію певного гену[13]. Цей принцип уже успішно використовується у лікуванні іншого генетичного захворювання — спінальної мязової атрофії.
Примітки ред.
- ↑ а б в г NDF-RT
- ↑ Drug Indications Extracted from FAERS — doi:10.5281/ZENODO.1435999
- ↑ Inxight: Drugs Database
- ↑ Subramaniam S, Sixt KM, Barrow R, Snyder SH (2009). Rhes, a Striatal Specific Protein, Mediates Mutant-Huntingtin Cytotoxicity. Science. 324 (5932): 1327—30. doi:10.1126/science.1172871. PMC 2745286. PMID 19498170.
- ↑ а б в Walker FO (2007). Huntington's disease. Lancet. 369 (9557): 218. doi:10.1016/S0140-6736(07)60111-1. PMID 17240289.
- ↑ Huntington Disease. genereviews bookshelf. University of Washington. 19 липня 2007. Архів оригіналу за 2 червня 2010. Процитовано 12 березня 2009.
- ↑ Kremer B (2002). Clinical neurology of Huntington's disease. У Bates G, Harper P, and Jones L (ред.). Huntington's Disease – Third Edition. Oxford: Oxford University Press. с. 28–53. ISBN 0-19-851060-8.
- ↑ Wagle, A C; Wagle SA, Marková IS, Berrios GE (2000). Psychiatric Morbidity in Huntington's disease. Neurology, Psychiatry and Brain Research (8): 5—16.
- ↑ Frank S, Jankovic J. (2010). Advances in the Pharmacological Management of Huntington's Disease. Drugs. 70 (5): 561—71. doi:10.2165/11534430-000000000-00000. PMID 20329804. Архів оригіналу за 8 жовтня 2011. Процитовано 12 жовтня 2012.
- ↑ FDA Approves First Drug for Treatment of Chorea in Huntington's Disease. FDA Approves First Drug for Treatment of Chorea in Huntington's Disease. U.S. Food and Drug Administration. 15 серпня 2008. Архів оригіналу за 1 червня 2012. Процитовано 10 серпня 2008.
- ↑ Walker FO (2007). Huntington's disease. Lancet. 369 (9557): 225. doi:10.1016/S0140-6736(07)60111-1. PMID 17240289.
{{cite journal}}: Вказано більш, ніж один|pages=та|page=(довідка) - ↑ Kirton Healthcare Group | High Quality Dynamic Seating Internationally Connected (en-GB) . Архів оригіналу за 25 вересня 2020. Процитовано 20 серпня 2020.
- ↑ Überarbeitetes Konzept für die Huntingtin-Verminderungsstudie von Roche - HDBuzz - Neuigkeiten aus der Huntington-Forschung. de.hdbuzz.net. Архів оригіналу за 24 жовтня 2020. Процитовано 20 серпня 2020.
Джерела ред.
- Джерело статті[недоступне посилання з листопадаа 2019]
- DMOZ HD links directory [Архівовано 25 лютого 2011 у Wayback Machine.] at the Open Directory Project.
- Huntington's Disease Outreach Project for Education, at Stanford (HOPES) [Архівовано 27 серпня 2020 у Wayback Machine.] — A layperson's guide to HD
- Worldwide Education and Awareness for Movement Disorders [Архівовано 11 жовтня 2009 у Wayback Machine.] — HD section
- European Huntington's Disease Network [Архівовано 28 липня 2009 у Wayback Machine.]